题目内容
【题目】误服铊盐会导致人体急性中毒,普鲁士蓝[KFe2(CN)6]可用作铊盐的解毒剂。
(1)Fe3+的价电子轨道表示式为___,与N同周期的主族元素中,第一电离能比N大的元素有___种。
(2)普鲁士蓝与硫酸作用可形成HCN,HCN的中心原子的杂化轨道类型为___,分子的立体构型是___,分子中σ键与π键数目之比为___。
(3)普鲁士蓝中的化学键不含有___(填字母)。
a.离子键
b.共价键
C.配位键
d.金属键
(4)已知FexCy的晶胞结构如图所示,则其化学式为___,铁原子的配位数是___。
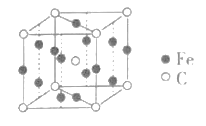
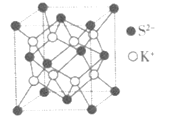
(5)如图为K2S的晶胞,该晶胞与CaF2晶胞结构相似,设晶体密度是ρg·cm-3,试计算K+与S2-的最短距离为___nm(阿伏加德罗常数用NA表示)。
【答案】![]() 1 sp 直线形 1:1 d Fe3C 2
1 sp 直线形 1:1 d Fe3C 2 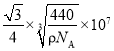
【解析】
(1)Fe是26号元素,电子排布式为1s22s22p63s23p63d64s2,因此Fe3+的价电子轨道表示式为![]() ,与N同周期的主族元素中,第一电离能比N大的元素有F共1种;故答案为:
,与N同周期的主族元素中,第一电离能比N大的元素有F共1种;故答案为:![]() ;1。
;1。
(2)HCN的中心原子价层电子对数为![]() ,其杂化轨道类型为sp,分子的立体构型是直线形,分子结构为H—C≡N,因此分子中σ键与π键数目之比为1:1;故答案为:sp;直线形;1:1。
,其杂化轨道类型为sp,分子的立体构型是直线形,分子结构为H—C≡N,因此分子中σ键与π键数目之比为1:1;故答案为:sp;直线形;1:1。
(3)a. 普鲁士蓝含有K+和[Fe2(CN)6]-,因此含有离子键,故a不符合题意;b. CN-含有共价键,故b不符合题意;c. [Fe2(CN)6]-含有配位键,故c不符合题意;d. 该离子化合物中不含金属键,故d符合题意;综上所述,答案为d。
(4)已知FexCy的晶胞结构如图所示,Fe的个数为![]() ,C的个数为
,C的个数为![]() ,则其化学式为Fe3C,以棱心的Fe分析,铁原子的配位数是2;故答案为:Fe3C;2。
,则其化学式为Fe3C,以棱心的Fe分析,铁原子的配位数是2;故答案为:Fe3C;2。
(5)如图为K2S的晶胞与CaF2晶胞结构相似,一个晶胞中有8个K+和4个S2,根据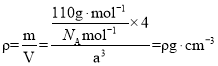 ,得到晶胞参数
,得到晶胞参数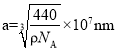 ,K+与S2的最短距离即为体对角线的四分之一,则
,K+与S2的最短距离即为体对角线的四分之一,则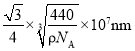 ;故答案为:
;故答案为: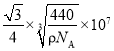 。
。