��Ŀ����
����Ŀ��������H����Ҫ���л������E��F��һ�������ºϳɣ�
��֪������Ϣ�� i��A���ڷ�������H����������
ii��I�ĺ˴Ź�������Ϊ����壬�ҷ�������Ϊ6:1��

�ش��������⣺
��1��E�Ĺ���������______________��B�Ľṹ��ʽ_____________��
��2��B �� C��G �� J�����ķ�Ӧ���� _______________��________________��
��3���� E + F �� H�Ļ�ѧ����ʽ_____________________��
�� I �� G �Ļ�ѧ����ʽ______________________��
��4��I��ͬϵ��K��I��Է���������28��K�ж���ͬ���칹�塣
��K��ͬ���칹�干_________________�֡�
����K���ܷ�����ȥ��Ӧ����K�Ľṹ��ʽΪ__________________��
���𰸡��Ȼ� ![]() ȡ����Ӧ��ˮ�ⷴӦ �Ӿ۷�Ӧ��ۺϷ�Ӧ
ȡ����Ӧ��ˮ�ⷴӦ �Ӿ۷�Ӧ��ۺϷ�Ӧ ![]() + CH3CH(OH)CH3
+ CH3CH(OH)CH3![]()
![]() + H2O
+ H2O ![]() +NaOH
+NaOH![]() CH2=CHCH3+NaCl����
CH2=CHCH3+NaCl����![]() �� 8 (CH3)3CCH2Cl
�� 8 (CH3)3CCH2Cl
��������
A���ڷ�����������ʽΪC7H8����AΪ![]() ��B�������ڹ��������·������ϵ�ȡ����Ӧ����B�����B�ķ���ʽ��֪BΪ
��B�������ڹ��������·������ϵ�ȡ����Ӧ����B�����B�ķ���ʽ��֪BΪ![]() ��B����ˮ�ⷴӦ����C��CΪ
��B����ˮ�ⷴӦ����C��CΪ![]() ��C��������������D��DΪ
��C��������������D��DΪ![]() ��D��������Һ��Ӧ���ữ�õ�E��EΪ
��D��������Һ��Ӧ���ữ�õ�E��EΪ![]() ��I�ķ���ʽΪC3H7Cl���˴Ź�������Ϊ����壬�ҷ�������Ϊ6��1����IΪCH3CHClCH3��I����ˮ�ⷴӦ�õ�F��FΪCH3CH(OH)CH3��E��F����������Ӧ����H��HΪ
��I�ķ���ʽΪC3H7Cl���˴Ź�������Ϊ����壬�ҷ�������Ϊ6��1����IΪCH3CHClCH3��I����ˮ�ⷴӦ�õ�F��FΪCH3CH(OH)CH3��E��F����������Ӧ����H��HΪ ��I������ȥ��Ӧ����GΪCH2=CHCH3��G�����Ӿ۷�Ӧ����J��JΪ
��I������ȥ��Ӧ����GΪCH2=CHCH3��G�����Ӿ۷�Ӧ����J��JΪ![]() ���ݴ˷������
���ݴ˷������
(1)ͨ�����Ϸ�����֪��EΪ![]() �����еĹ�����Ϊ�Ȼ���B�ṹ��ʽΪ
�����еĹ�����Ϊ�Ȼ���B�ṹ��ʽΪ![]() ���ʴ�Ϊ���Ȼ���
���ʴ�Ϊ���Ȼ���![]() ��
��
(2)��������������B����ˮ�ⷴӦ����C��B��CΪȡ����Ӧ��G�����Ӿ۷�Ӧ����J��G��JΪ�Ӿ۷�Ӧ���ʴ�Ϊ��ȡ����Ӧ���Ӿ۷�Ӧ��
(3)��E+F��H�Ļ�ѧ����ʽΪ��![]() + CH3CH(OH)CH3
+ CH3CH(OH)CH3![]()
![]() + H2O����I��G �Ļ�ѧ����ʽ��
+ H2O����I��G �Ļ�ѧ����ʽ��![]() +NaOH
+NaOH![]() CH2=CHCH3+NaCl ��
CH2=CHCH3+NaCl ��![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() + CH3CH(OH)CH3
+ CH3CH(OH)CH3![]()
![]() + H2O��
+ H2O��![]() +NaOH
+NaOH![]() CH2=CHCH3+NaCl(��
CH2=CHCH3+NaCl(��![]() )��
)��
(4)I(CH3CHClCH3)��ͬϵ��K��I��Է���������28����K�ķ���ʽΪC5H11Cl��
�ٿ��Կ���C5H12��ȡ�������������һ����ԭ�ӱ���ԭ��ȡ����3�֣���������һ����ԭ�ӱ���ԭ��ȡ����4�֣���������һ����ԭ�ӱ���ԭ��ȡ����1�֣���K��ͬ���칹����8�֣��ʴ�Ϊ��8��
����K���ܷ�����ȥ��Ӧ��˵������ԭ��ֱ��������̼ԭ�ӵ���λ̼ԭ����û����ԭ�ӣ���K�Ľṹ��ʽΪ(CH3)3CCH2Cl���ʴ�Ϊ��(CH3)3CCH2Cl��

����Ŀ������һ��������ܱ������У��������»�ѧ��Ӧ��CO2��g����H2��g��![]() CO��g����H2O��g�����仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
CO��g����H2O��g�����仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
t�� | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
�ش��������⣺
��1���÷�ӦΪ____________��Ӧ��ѡ�����ȡ����ȣ���
��2�����жϸ÷�Ӧ�Ƿ�ﵽ��ѧƽ��״̬��������_________��
a��������ѹǿ���� b����������� c��CO������
c��������H2����������H2O�� d��c��CO2����c��CO��
��3��ij�¶��£�ƽ��Ũ�ȷ�����ʽ��c��CO2����c��H2����c��CO����c��H2O�������жϴ�ʱ���¶�Ϊ _________�档
����һ���������ܱ������г���2 mol A��0.6 mol C��һ������B�������壬һ�������·�����Ӧ2A(g)+B(g) ![]() 3C(g)�������ʵ�Ũ����ʱ��仯�Ĺ�ϵ��ͼ1��ʾ��������t0��t1��c(B)δ������ͼ2Ϊ��Ӧ��ϵ�з�Ӧ������ʱ��仯���������t2��t3��t4���ı�һ����ͬ��������
3C(g)�������ʵ�Ũ����ʱ��仯�Ĺ�ϵ��ͼ1��ʾ��������t0��t1��c(B)δ������ͼ2Ϊ��Ӧ��ϵ�з�Ӧ������ʱ��仯���������t2��t3��t4���ı�һ����ͬ��������
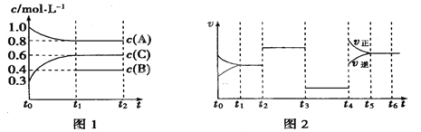
��1����t1=15 min����t0��t1����C��Ũ�ȱ仯��ʾ�ķ�Ӧ����V(C)=_____��
��2��t3ʱ�ı������Ϊ___________��B����ʼ���ʵ���Ϊ_______��
��3��t4��t5�Σ���A�����ʵ���������0.01 mol�����˽��з�Ӧ��ϵ��������Ϊa kJ��д���������¸÷�Ӧ���Ȼ�ѧ����ʽ___________________��