题目内容
【题目】在实验室里,用足量的浓盐酸与一定量的MnO2反应,来制取氯气。
⑴用“双线桥法”标出电子转移情况
MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
⑵若生成2.24L标准状况时的氯气,请计算(写出必要的计算过程):
①理论上需要多少克MnO2参加反应?
②被氧化的HCl的物质的量为多少?
【答案】(1)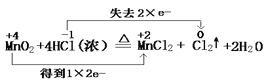
(2)① 8.7g(3分) ②0.2mol(3分)
【解析】
试题分析:(1)根据方程式可知Mn元素的化合价从+4价降低到+2价,得到2个电子,Cl元素化合价从-1价升高到0价,失去1个电子,因此电子转移用双线桥可表示为(见答案);
(2)MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
87g 被氧化2mol 22.4L
m(MnO2) n(HCl) 2.24L
①m(MnO2)=(87g×2.24L)/22.4L=8.7g(3分)
②n(HCl) =(2mol×2.24L)/22.4L=0.2mol(3分)

练习册系列答案
相关题目