题目内容
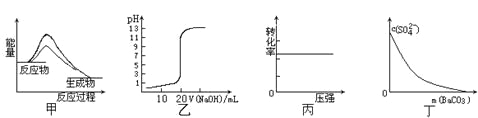
【题目】在一恒温恒压的密闭容器中发生如下反应:A(g)+B(g)2C(g) △H<0,t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程如图所示。下列说法不正确的是( )
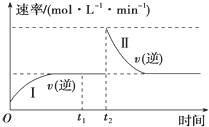
A.0~t2时,v(正)>v(逆)
B.Ⅰ、Ⅱ两过程达到平衡时,A的体积分数Ⅰ=Ⅱ
C.t2时刻改变的条件是向密闭容器中加C
D.Ⅰ、Ⅱ两过程达到平衡时,平衡常数K(Ⅰ)=K(Ⅱ)
【答案】A
【解析】
![]() 过程Ⅰ,0~t1,逆反应速率增大过程中,反应正向进行,则
过程Ⅰ,0~t1,逆反应速率增大过程中,反应正向进行,则![]() ,t1~t2,逆反应速率不变时,反应到达平衡,则
,t1~t2,逆反应速率不变时,反应到达平衡,则![]() ,故A错误,符合题意;
,故A错误,符合题意;
B.![]() 时刻改变条件后,再次达到平衡时逆反应速率不变,说明和原平衡等效,A的体积分数Ⅰ
时刻改变条件后,再次达到平衡时逆反应速率不变,说明和原平衡等效,A的体积分数Ⅰ![]() Ⅱ,故B正确,不符合题意;
Ⅱ,故B正确,不符合题意;
C.密闭容器中加C,逆反应速率瞬间增大,恒温恒压下与原平衡为等效平衡,故C正确,不符合题意;
D.平衡常数只受温度影响,Ⅰ、Ⅱ两过程为等效平衡,温度相同,Ⅰ、Ⅱ两过程达到平衡时,平衡常数K(Ⅰ)=K(Ⅱ),故D正确,不符合题意;
故选:A。

 应用题作业本系列答案
应用题作业本系列答案 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案【题目】下列实验内容能达到实验目的的是
实验目的 | 实验内容 | |
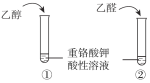
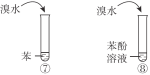
A | 鉴别乙醇与乙醛 |
|
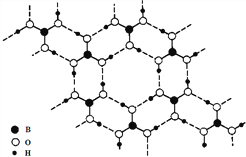
B | 比较乙酸、碳酸、苯酚的酸性 |
|
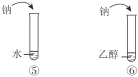
C | 说明烃基对羟基上氢原子活性的影响 | |
D | 说明苯环对取代基上氢原子活性的影响 |
|
A. AB. BC. CD. D
【题目】向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:xA(g)+B(g) ![]() 2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下表和下图表示
2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下表和下图表示
容器 | 甲 | 乙 | 丙 |
容积 | 0.5L | 0.5L | 1.0L |
温度/℃ | T1 | T2 | T2 |
反应物起始量 | 0.5molA 1.5 molB | 0.5 molA 1.5 molB | 2.0 molA 6.0 molB |
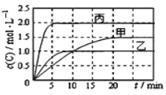
下列说法正确的是
A.由图可知:T1<T2,且该反应为吸热反应
B.T2时该反应的平衡常数K=0.8
C.l0min内甲容器中反应的平均速率v(B)=0.025mol·(L·min)-1
D.T1℃,若起始时甲容器中充入1.5molA、0.5molB,平衡时B的转化率为25%