题目内容
【题目】明矾石是制取钾肥和氢氧化铝的重要原料,明矾石的组成和明矾相似,此外还含有氧化铝和少量的氧化铁杂质。具体实验流程如下:
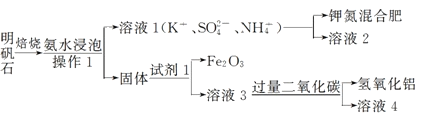
请回答下列问题:
(1)操作l所用到的玻璃仪器的名称是______________________。
(2)由溶液3制取氢氧化铝的离子方程式为__________。
(3)明矾石焙烧时产生SO2气体,请你写出能验证SO2气体具有还原性且实验现象明显的化学方程式________________________。
(4)请你写出验证溶液l中有NH4+的实验过程___________。
(5)实验室用Fe2O3与CO反应来制取单质Fe。
①请你按气流由左到右方向连接下列各装置,顺序为:A→_________________。
②检验装置A气密性的方法是______________________。
③在点燃B处的酒精灯前,应进行的操作是____________________。
④装置C的作用是_________________________。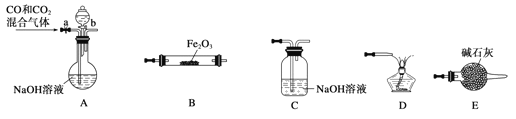
【答案】漏斗、烧杯、玻璃棒 AlO2+CO2+H2O=Al(OH)3+HCO3 SO2+Cl2+H2O=H2SO4+HCl 取少量溶液1于试管中,加入浓氢氧化钠溶液加热,有能使湿润的红色石蕊试纸变蓝的气体生成,证明溶液1中含有NH4+ E→B→C→D 关闭a、b两处活塞,将导气管插入水槽中,微热,导气管口有气泡产生,停止微热,一段时间后,导管中形成一段水柱,说明气密性良好 检验CO气体纯度 除去CO气体混有的二氧化碳,利用CO点燃
【解析】
(1)将液体和不溶于液体的固体分离开来的操作是过滤;
(2)明矾石的组成和明矾相似,还含有氧化铝和少量的氧化铁杂质,可知固体为氢氧化铝、氧化铝、氧化铁.试剂1将铝元素转化到溶液3中,并将氧化铁除掉,所以试剂1为强碱,溶液3中含有偏铝酸根,通入二氧化碳,生成氢氧化铝沉淀;
(3)二氧化硫可与氧化性的氯水、溴水和酸性高锰酸钾反应,据此分析作答;
(4)铵根离子与强碱反应,转化为氨气,氨气能使湿润的红色石蕊试纸变蓝;
(5)①根据各部分装置的作用连接;
②利用气体的热胀冷缩;
③CO为易燃气体,加热要检验其纯度;
④CO有毒,直接排放空气中,污染大气,通过燃烧方法转化为二氧化碳,从B中出来的气体含有二氧化碳,不利于CO点燃。
(1)将液体和不溶于液体的固体分离开来的操作是过滤,过滤用到的玻璃仪器为漏斗、烧杯、玻璃棒,
故答案为漏斗、烧杯、玻璃棒;
(2)溶液3中含有偏铝酸根,通入过量二氧化碳,反应生成氢氧化铝沉淀与碳酸氢根离子,反应离子方程式为AlO2+CO2+H2O=Al(OH)3+HCO3;
(3) 能验证SO2气体具有还原性且实验现象明显的化学方程式为SO2+Cl2+H2O=H2SO4+HCl;
(4) 验证溶液l中有NH4+的实验操作为:取少量溶液1于试管中,加入浓氢氧化钠溶液加热,有能使湿润的红色石蕊试纸变蓝的气体生成,证明溶液1中含有NH4+,
故答案为取少量溶液1于试管中,加入浓氢氧化钠溶液加热,有能使湿润的红色石蕊试纸变蓝的气体生成,证明溶液1中含有NH4+;
(5)①A作用除去CO中混有的二氧化碳,B为Fe2O3与CO反应装置,C作用为吸收从B中出来的气体混有的二氧化碳,D作用为燃烧剩余的CO,E作用为干燥进入B装置的气体。所以各装置顺序为:A→E→B→C→D;
②利用气体的热胀冷缩检验气密性。操作为:关闭a、b两处活塞,将导气管插入水槽中,微热,导气管口有气泡产生,停止微热,一段时间后,导管中形成一段水柱,说明气密性良好,
故答案为关闭a、b两处活塞,将导气管插入水槽中,微热,导气管口有气泡产生,停止微热,一段时间后,导管中形成一段水柱,说明气密性良好;
③CO为易燃气体,不纯受热会发生爆炸危险,所以在加热前要检验其纯度,
故答案为检验CO气体纯度;
④从B中出来的气体含有二氧化碳,不利于CO点燃,C装置作用为除去CO气体混有的二氧化碳,利用CO点燃,
故答案为除去CO气体混有的二氧化碳,利用CO点燃。