题目内容
【题目】已知:①A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平;现以A为主要原料合成乙酸乙酯,其合成路线如图所示.
(1)C的结构简式为 , D中的官能团名称分别为
(2)写出①的化学方程式: , 反应类型
(3)写出④的化学方程式 , 反应类型为 .
【答案】
(1)CH3CHO;羧基
(2)CH2=CH2+H2O ![]() CH3CH2OH;加成反应
CH3CH2OH;加成反应
(3)CH3CH2OH+CH3COOH ![]() CH3COOCH2CH3+H2O;酯化反应
CH3COOCH2CH3+H2O;酯化反应
【解析】解:A的产量通常用来衡量一个国家的石油化工水平,则A为CH2=CH2 , 与水发生加成反应得到B为CH3CH2OH,乙醇和乙酸发生酯化反应生成乙酸乙酯,所以D为CH3COOH,乙醇被催化氧化生成乙醛,乙醛被氧化生成乙酸,所以C为CH3CHO.
(1)C为CH3CHO,D为CH3COOH,D中的官能团名称为羧基,所以答案是:CH3CHO;羧基;
(2)反应①为乙烯和水的加成反应,反应方程式CH2=CH2+H2O ![]() CH3CH2OH,④为乙醇与乙酸的酯化反应,反应方程式CH3CH2OH+CH3COOH
CH3CH2OH,④为乙醇与乙酸的酯化反应,反应方程式CH3CH2OH+CH3COOH ![]() CH3COOCH2CH3+H2O,
CH3COOCH2CH3+H2O,
所以答案是:CH2=CH2+H2O ![]() CH3CH2OH,加成反应;CH3CH2OH+CH3COOH
CH3CH2OH,加成反应;CH3CH2OH+CH3COOH ![]() CH3COOCH2CH3+H2O,酯化反应.
CH3COOCH2CH3+H2O,酯化反应.

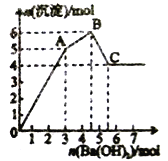
【题目】向FeCl3、Al2(SO4)3的混合溶液中逐滴加入Ba(OH)2溶液,形成沉淀的情况如图所示。
氢氧化物 | 溶液pH | |||
开始沉淀 | 沉淀完全 | 沉淀开始溶解 | 沉淀完全溶解 | |
Fe(OH)3 | 2.3 | 3.4 | - | - |
A1(OH)3 | 3.3 | 5.2 | 7.8 | 12.8 |
A. 据图计算原溶液中c(Cl-)>c(SO42-)
B. C点的沉淀为Fe (OH)3
C. AB段可能发生的反应是:2SO42-+ 2Ba2+ + Al3+ + 3OH- == 2BaSO4↓ + A1(OH)3↓
D. OA段可能发生的反应是:3Ba2+ + 6OH- + 3SO42- + Fe3+ + Al3+ = 3BaSO4↓ + Fe (OH)3↓ + A1(OH)3↓
