题目内容
标准状况下有①6.72L甲烷②3.01×1023个氯化氢分子③13.6gH2S气体④0.2mol氨
气。下列对这四种气体的关系从小到大顺序排列(用序号表示)
| A.体积______________________________ | B.密度__________________________ |
| C.质量______________________________ | D.氢原子数______________________ |
解析试题分析: CH4的物质的量是n=V/Vm=6.72/22.4=0.3mol。HCl的物质的量是n=N/NA=3.01*10^23/6.02*10^23=0.5mol。H2S的物质的量是n=m/M=13.6/34=0.4mol。0.2mol NH3
同温同压下,体积比等于物质的量之比,故④<①<③<②。
同温同压下,密度之比等于摩尔质量之比,故①<④<③<②
质量等于物质的量乘以摩尔质量,故④<①<③<②
0.3mol CH4中含氢原子物质的量为1.2mol, 0.5molHCl中含氢原子物质的量为0.5mol, 0.4molH2S含氢原子物质的量为0.8mol,0.2mol NH3含氢原子物质的量为0.6mol.则氢原子数:②<④<③<①
考点:考查物质的量计算的相关知识点。

 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案下列有关化学用语表示正确的是
| A.Mg2+的电子排布式:1s22s22p63s2 |
B.铁的原子结构示意图: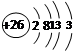 |
C.Na2S的电子式: 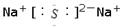 |
| D.次氯酸的结构式:H-Cl-O |
下列说法正确的是( )
| A.摩尔是七个基本物理量之一 |
| B.1mol氢 |
| C.摩尔是表示物质的数量单位 |
| D.每摩尔物质都含有阿伏加德罗常数个指定微粒 |
用NA表示阿伏加德罗常数,下列叙述正确的是
| A.46 g乙醇中含有的化学键数为7 NA |
| B.1 mol氯气和足量NaOH溶液反应转移电子数为2 NA |
| C.1 mol OH-和1 mol -OH(羟基)中含有的质子数均为 9 NA |
| D.10 L 0.1 mol·L-1的Na2CO3溶液中,Na+、CO32-总数为3 NA |
NA代表阿伏加德罗常数,下列说法正确的是( )
| A.标准状况下,22.4 LSO3中含有的分子数为NA |
| B.100 mL 2.0 mol/L的盐酸与醋酸溶液中氢离子均为0.2NA |
| C.0.1mol/L稀硫酸中含SO42-的数目为0.1NA |
| D.标准状况下,11.2LNO和5.6LO2混合后,分子总数小于0.5NA |
已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:
(1)该“84消毒液”的物质的量浓度约为 mol·L-1。
(2)某同学取100 mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)= mol·L-1。
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480 mL含NaClO质量分数为25%的消毒液。下列说法正确的是 (填序号)。
| A.如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器 |
| B.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制 |
| C.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低 |
| D.需要称量NaClO固体的质量为143.0 g |

(4)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.84 g·cm-3)的浓硫酸配制2 000 mL 2.3 mol·L-1的稀硫酸用于增强“84消毒液”的消毒能力。
①所配制的稀硫酸中,H+的物质的量浓度为 mol·L-1。
②需用浓硫酸的体积为 mL。
钠是活泼的碱金属元素,钠及其化合物在生产和生活中有广泛的应用。
完成下列计算:
(1)叠氮化钠(NaN3)受撞击完全分解产生钠和氮气,故可应用于汽车安全气囊。若产生40.32 L(标准状况下)氮气,至少需要叠氮化钠________g。
(2)钠钾合金可在核反应堆中用作热交换液。5.05 g钠钾合金溶于200 mL水生成0.075 mol氢气。
①计算溶液中氢氧根离子的物质的量浓度(忽略溶液体积变化)。
_____________________________________________________________
②计算并确定该钠钾合金的化学式。
_____________________________________________________________
(3)氢氧化钠溶液处理铝土矿并过滤,得到含铝酸钠的溶液。向该溶液中通入二氧化碳,有下列反应:
2NaAlO2+3H2O+CO2=2Al(OH)3↓+Na2CO3
已知通入二氧化碳336 L(标准状况下),生成24 mol Al(OH)3和15 mol Na2CO3,若通入溶液的二氧化碳为112 L(标准状况下),计算生成的Al(OH)3和Na2CO3的物质的量之比。
_________________________________________________________________
(4)常温下,称取不同氢氧化钠样品溶于水,加盐酸中和至pH=7,然后将溶液蒸干得氯化钠晶体,蒸干过程中产品无损失。
| | 氢氧化钠质量(g) | 氯化钠质量(g) |
| ① | 2.40 | 3.51 |
| ② | 2.32 | 2.34 |
| ③ | 3.48 | 3.51 |
上述实验①②③所用氢氧化钠均不含杂质,且实验数据可靠。通过计算,分析和比较上表3组数据,给出结论。