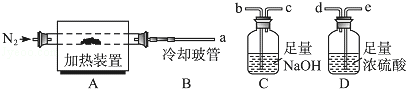
题目内容
NA代表阿伏加德罗常数,下列说法正确的是( )
| A.标准状况下,22.4 LSO3中含有的分子数为NA |
| B.100 mL 2.0 mol/L的盐酸与醋酸溶液中氢离子均为0.2NA |
| C.0.1mol/L稀硫酸中含SO42-的数目为0.1NA |
| D.标准状况下,11.2LNO和5.6LO2混合后,分子总数小于0.5NA |
D
解析试题分析:标准状况下,三氧化硫不是气体,不能适用于气体摩尔体积,A不正确;盐酸是强酸,完全电离。醋酸是弱酸,存在电离平衡,则100 mL 2.0 mol/L的醋酸溶液中氢离子小于0.2NA,B不正确;C中不能确定稀硫酸的体积,无法计算硫酸的物质的量,C不正确;标准状况下,11.2LNO和5.6LO2混合后,二者恰好反应生成0.5molNO2,但NO2存在化学平衡,即2NO2 N2O4,所以分子总数小于0.5NA,D正确,答案选D。
N2O4,所以分子总数小于0.5NA,D正确,答案选D。
考点:考查阿伏加德罗常数的有关计算和判断
点评:阿伏加德罗常数是历年高考的“热点”问题,这是由于它既考查了学生对物质的量、粒子数、质量、体积等与阿伏加德罗常数关系的理解,又可以涵盖多角度的化学知识内容。要准确解答好这类题目,一是要掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系;二是要准确弄清分子、原子、原子核内质子中子及核外电子的构成关系。

练习册系列答案
相关题目
正确掌握化学用语是学好化学的基础。下列化学用语中正确的是
| A.乙烯的结构简式为CH2CH2 | B.乙醇的结构简式为C2H6O |
| C.丙烷的实验式为 C3H8 | D.羟基的电子式: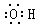 |
下列化学用语正确的是 ( )
| A.1,2—二溴乙烷的结构简式:C2 H4 Br2 |
| B.羟基的化学式:OH- |
| C.己烷的分子式:C6H12 |
| D.乙烯分子的最简式:CH2 |
用NA表示阿伏加德罗常数,下列叙述正确的是
| A.2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA |
| B.0.5molC3H8分子中所含C-H共价键数为2NA |
| C.标准状况下,22.4L乙醇完全燃烧所耗的氧气分子数为3NA |
| D.1mol碳正离子CH5+所含的电子数为11NA |
下列有关化学用语使用正确的是( )
A.CO2的电子式: |
B.核内有8个中子的碳原子: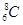 |
C.钾原子结构示意图: |
D.乙烯的比例模型: |
标准状况下有①6.72L甲烷②3.01×1023个氯化氢分子③13.6gH2S气体④0.2mol氨
气。下列对这四种气体的关系从小到大顺序排列(用序号表示)
| A.体积______________________________ | B.密度__________________________ |
| C.质量______________________________ | D.氢原子数______________________ |
已知硫酸、氨水的密度与所加水量的关系如图所示,现有硫酸与氨水各一份,请根据表中信息,回答下列问题: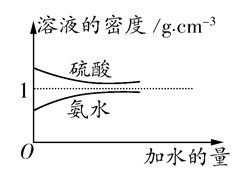
| | 溶质的物质的量 浓度(mol·L-1) | 溶液的密度(g·cm-3) |
| 硫酸 | c1 | ρ1 |
| 氨水 | c2 | ρ2 |
(1)表中硫酸的质量分数为 (不写单位,用含c1、ρ1的代数式表示)。
(2)物质的量浓度为c1 mol·L-1的硫酸与水等体积混合(混合后溶液体积变化忽略不计),所得溶液的物质的量浓度为 mol·L-1。
(3)物质的量浓度为c2 mol·L-1的氨水与
 c2 mol·L-1的氨水等质量混合,所得溶液的密度 (填“大于”、“小于”或“等于”,下同)ρ2 g·cm-3,所得溶液的物质的量浓度
c2 mol·L-1的氨水等质量混合,所得溶液的密度 (填“大于”、“小于”或“等于”,下同)ρ2 g·cm-3,所得溶液的物质的量浓度 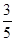 c2 mol·L-1(设混合后溶液的体积变化忽略不计)。
c2 mol·L-1(设混合后溶液的体积变化忽略不计)。