题目内容
【题目】在3NO2+H2O=2HNO3+NO中,氧化剂与还原剂的物质的量比为( )
A.1∶2B.2∶1C.1∶3D.3∶1
【答案】A
【解析】
该反应中N元素化合价由NO2中的+4价变为NO的+2价、HNO3的+5价,化合价降低的NO2是氧化剂、化合价升高的NO2是还原剂,化合价降低的NO2的计量数是1、化合价升高的NO2的计量数是2,所以氧化剂和还原剂的物质的量之比为1:2,故合理选项是A。

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目
【题目】下图是元素周期表的一部分,根据元素在周期表中的位置回答下列问题,
① | ② | ③ | |||||||||||||||
④ | ⑤ | ⑥ | |||||||||||||||
⑦ | ⑧ | ⑨ | |||||||||||||||
⑩ | |||||||||||||||||
(1)元素⑤在周期表中的位置描述为____________,元素⑧的元素符号__________________。
(2)元素①~⑩的最高价氧化物的水化物中,碱性最强的是________________(填化学式)。
(3)元素②的单质的电子式______________,元素②的简单氢化物与其最高价氧化物的水化物反应,生成物中含有的化学键________________(填“离子键”、“极性键”或“非极性键”),元素①、②、③的简单氢化物的沸点由高到低的顺序是___________________(用化学式表示)。
(4)非金属性比较
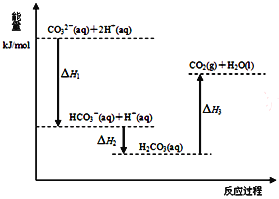
a.装置1可用于比较元素①、②、⑤的非金属性强弱,则B中发生反应的离子方程式为:_______。
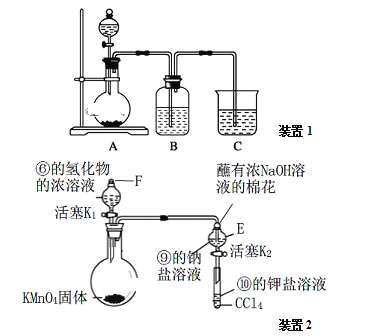
b.打开装置2中玻璃塞F和活塞K1,使液体滴入烧瓶中,待E中溶液颜色不再变化后,打开活塞K2,将E中溶液滴入小试管中,关闭活塞K2,取下小试管振荡,静置,下层液体呈现紫红色。上述实验_______(填“能”或“不能”)证明非金属性⑥>⑨>⑩。