题目内容
2.下列有关金属腐蚀及其防护的叙述 中不正确的是( )| A. | 金属的电化学腐蚀比化学腐蚀更普遍 | |
| B. | 用牺牲锌块的方法来保护船身 | |
| C. | 用铜质铆钉铆接铁板,铁板不易被腐蚀 | |
| D. | 浸泡在水中钢闸门,水面附近区域的腐蚀程度大于长期在水下的部分 |
分析 A、金属的腐蚀以电化学腐蚀更普遍;
B、锌的活泼性大于铁,形成原电池时锌作负极被腐蚀;
C、金属铁和铝形成的原电池中,活泼的金属铝为负极,更易被腐蚀;
D、能形成原电池且作原电池负极的金属加速被腐蚀.
解答 解:A、在日常生活的金属腐蚀中,以电化学腐蚀更为普遍,故A正确;
B、锌的活泼性大于铁,用牺牲锌块的方法来保护船身而防止铁被腐蚀,故B正确;
C、金属铁和铝形成的原电池中,活泼的金属铝为负极,更易被腐蚀,金属铁被保护,故C错误;
D、在空气与水面交接处溶解的氧气比水下多,铁、碳和溶于氧气的水能构成原电池,铁易失电子而作负极,作负极的金属加速被腐蚀,所以与水面交接处的钢柱,比在水下部分的钢柱容易腐蚀,故D正确.
故选C.
点评 本题考查学生金属腐蚀的原理以及原电池的工作原理和金属的保护知识,注意基本知识的梳理和归纳很关键,难度不大.

练习册系列答案
相关题目
12.下列四种元素中,其单质氧化性最强的是( )
| A. | 基态原子含有未成对电子最多的第二周期元素 | |
| B. | 基态原子电子排布式为[Ne]3s23p1的元素 | |
| C. | 基态原子最外电子层排布为2s22p6的元素 | |
| D. | 基态原子最外电子层排布为3s23p5的元素 |
13.描述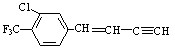 分子的下列叙述中,错误的是( )
分子的下列叙述中,错误的是( )
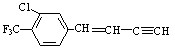 分子的下列叙述中,错误的是( )
分子的下列叙述中,错误的是( )| A. | 与苯环直接相连的原子都在同一平面上 | |
| B. | 分子中的碳原子分别采取sp、sp2、sp3杂化,分子中共有10个不饱和碳原子 | |
| C. | 最多有18个原子可能处在同一个平面上 | |
| D. | 分子式为C11H6ClF3 |
10.下列说法或表示法正确的是( )
| A. | 在稀溶液中:H++OH-═H2O;△H=-57.3kJ/mol,若将含0.5mol H2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热量等于57.3kJ | |
| B. | 由4P(s,红磷)═P4(s,白磷):△H>0可知,白磷的热稳定性比红磷大 | |
| C. | 已知2H2(g)+O2(g)═2H2O(g);△H=-483.6kJ•mol-1,则H2的燃烧热等于241.8 kJ•mol-1 | |
| D. | 己知:S(g)+O2(g)═SO2(g);△H1及S(s)+O2(g)═SO2(g):△H2,则△H1<△H2 |
17.下列化学式只能表示一种纯净物的是( )
| A. | CHFBrI | B. | C2H4O2 | C. | C6H12O6 | D. | CF2Cl2 |
7.下列有关同分异构体数目的叙述中,正确的是( )
| A. | 甲苯苯环上的一个氢原子被含4个碳原子的烷基取代,所得产物有12种 | |
| B. | 等物质的量的氯气与乙烷在光照条件下反应得到9种产物 | |
| C. | 已知二氯苯有3种同分异构体,则四氯苯的同分异构体的数目为6种 | |
| D. | 苯乙烯和氢气完全加成的产物的一溴取代物有5种 |
14.下列叙述不正确的是( )
| A. | 热的纯碱溶液可以去除餐具上的油污 | |
| B. | 过氧化钠可用做呼吸面具的供氧剂 | |
| C. | 工业上用电解饱和食盐水获得金属钠 | |
| D. | 氢氧化铝是医用的胃酸中和剂的一种 |
11.下列离子方程式正确的是( )
| A. | 乙酸与碳酸钠溶液反应:2H++CO32-═CO2↑+H2O | |
| B. | 乙醇与钠反应:2CH3CH2O-+2H++2Na→2CH3CH2ONa+H2↑ | |
| C. | 苯酚钠溶液中通入二氧化碳:2C6H5O-+CO2+H2O→2C6H5OH+CO32- | |
| D. | 苯酚溶液中加入溴水: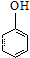 +3B2→ +3B2→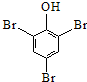 ↓+3H++3Br- ↓+3H++3Br- |
 ,电子排布式1s22s22p63s23p63d14s2.该元素的原子序数为21,该元素是金属元素(填“金属”或“非金属”),形成的单质为金属晶体.
,电子排布式1s22s22p63s23p63d14s2.该元素的原子序数为21,该元素是金属元素(填“金属”或“非金属”),形成的单质为金属晶体.