题目内容
【题目】某化学实验小组欲用下列装置制备纯净的氯气及含氯化物,并探究其性质。
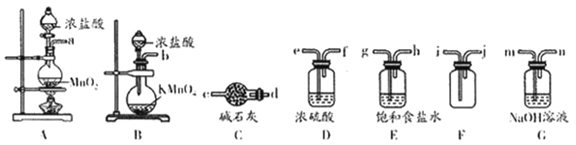
(1)欲制备并收集一瓶纯净的氯气,选择上图中合适的装置,其连接顺序为:__________________(按气流方向,用小写字母表示)。根据选择的装置,写出制备氯气的化学方程式_______________________。
(2)取100mL氯气与NaOH溶液反应生成的“84”消毒液,持续通入过量的SO2,溶液中开始出现黄绿色,后黄绿色逐渐褪去。溶液变为黄绿色的可能原因是:
①溶液中Cl-与ClO-反应所致,设计实验方案确认这种可能性:________________。
②_________________所致(用离子方程式表示)。
向反应后的溶液中先加入足量稀盐酸,再加入足量氯化钡溶液,经过滤、洗涤、干燥、称量,所得沉淀的质量为w g,则溶液中NaC1O的物质的量浓度为________mol·L-1。
(3)在加热条件下,氯气与NaOH溶液反应生成NaC1O3和NaC1等,写出反应的离子方程式___________________。
实验小组设计下图装置(加热装置略去)验证NaClO3的性质。
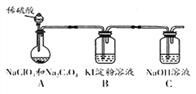
已知:2NaClO3+Na2C2O4+2H2SO4(稀)=2C1O2↑+2CO2↑+2Na2SO4+2H2O;C1O2与氯气的化学性质相似。控制装置A中分液漏斗活塞,缓慢滴加稀硫酸,观察到B装置中的现象是_____________;装置C吸收的物质是 ___________________。
【答案】 a(或b)、g、h、e、f、i、j、d(或m) a对应:MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
b对应:2KMnO4+16HCl=2KCl+MnCl2+5Cl2↑+8H2O 取少量“84”消毒液于试管中,滴加稀硫酸,观察溶液颜色变为黄绿色 2ClO-+SO2=Cl2+SO42- ![]() 3Cl2+6OH-=ClO3-+5Cl-+3H2O 溶液变蓝 ClO2和CO2
3Cl2+6OH-=ClO3-+5Cl-+3H2O 溶液变蓝 ClO2和CO2
【解析】(1)欲制备并收集一瓶纯净的氯气,二氧化锰固体和浓盐酸在加热条件下生成氯气,该反应为固液反应,需要加热,选a制Cl2,KMnO4固体和浓盐酸在不加热条件下就能生成氯气,该反应为固液反应,不需要加热,选b制Cl2,E除HCl,D干燥,F收集Cl2,C或G除去尾气,故选用装置连接顺序为 a(或b)、g、h、e、f、i、j、d(或m),a对应:MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O,b对应:2KMnO4+16HCl=2KCl+MnCl2+5Cl2↑+8H2O ;(2)①取少量“84”消毒液于试管中,滴加稀硫酸,观察溶液颜色变为黄绿色 ②反应的离子方程式为2ClO-+SO2=Cl2+SO42- ;
MnCl2+Cl2↑+2H2O,b对应:2KMnO4+16HCl=2KCl+MnCl2+5Cl2↑+8H2O ;(2)①取少量“84”消毒液于试管中,滴加稀硫酸,观察溶液颜色变为黄绿色 ②反应的离子方程式为2ClO-+SO2=Cl2+SO42- ;
NaClO~SO42- ~BaSO4
1mol 233g
x w g
x=w/233mol
c(ClO― )= ![]() ;
;
(3)在加热条件下,氯气与NaOH溶液反应生成NaClO3,3Cl2+6OH-=ClO3-+5Cl-+3H2O;控制装置A中分液漏斗活塞,缓慢滴加稀硫酸,ClO2将I― 氧化为I2,I2能使淀粉溶液呈蓝色,观察到B装置中的现象是溶液变蓝,装置C吸收的物质是ClO2和CO2。
