题目内容
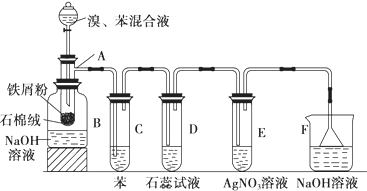
15.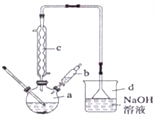 实验室制备溴苯的实验步骤如下:
实验室制备溴苯的实验步骤如下:步骤1:在a中加入苯和少量铁屑,将b中液溴慢慢加入到a中,充分反应;
步骤2:反应结束后,冷却至常温过滤反应液;
步骤3:滤液用水洗后再用10%的NaOH溶液洗,得粗溴苯;
步骤4:向粗溴苯中加入少量无水氯化钙,静置、过滤.
回答下列问题:
(1)仪器a中铁屑的作用是催化剂,a中发生的主要反应方程式是
 +Br2$\stackrel{Fe}{→}$
+Br2$\stackrel{Fe}{→}$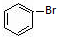 +HBr.
+HBr.(2)仪器c的作用是冷凝回流.
(3)步骤3中用水洗涤除去的物质是FeBr3,后用NaOH溶液洗涤除去的物质是Br2.
(4)步骤4得到的粗溴苯中还含有杂质苯和少量对二溴苯等,下表是有关物质的物理性质数据,为了得到纯净的溴苯,还必须要进行的实验名称是蒸馏.
| 苯 | 溴苯 | 对二溴苯 | |
| 密度/gcm-3 | 0.88 | 1.50 | 1.96 |
| 沸点/℃ | 80 | 156 | 220 |
| 水溶性 | 微溶 | 微溶 | 难溶 |
分析 步骤1:在a中加入苯和少量铁屑,将b中液溴慢慢加入到a中,充分反应,在Fe作催化剂条件下,苯和溴发生取代反应生成溴苯,同时有HBr生成,溴具有挥发性,所以生成的HBr中含有溴单质;
步骤2:反应结束后,冷却至常温过滤反应液,滤去难溶性固体;
步骤3:滤液用水洗,洗去生成的FeBr3,溴易溶于溴苯中,所以粗溴苯中含有溴单质,溴能和NaOH反应但溴苯和NaOH不反应,用NaOH溶液除去溴苯中的溴,从而得到粗溴苯;
步骤4:向粗溴苯中加入少量无水氯化钙,静置、过滤,氯化钙具有吸水性,作干燥剂;
HBr不能直接排空,且能和NaOH反应,所以用NaOH溶液除去HBr.
(1)在苯和溴的取代反应中,Fe作催化剂;在Fe作催化剂条件下,苯和溴发生取代反应生成溴苯,同时有HBr生成;
(2)仪器c是冷凝管,冷凝管有冷凝回流作用;
(3)步骤3中用水洗涤除去可溶性杂质,后用NaOH溶液洗涤除去溴;
(4)分离互溶性液体应该采用蒸馏方法.
解答 解:步骤1:在a中加入苯和少量铁屑,将b中液溴慢慢加入到a中,充分反应,在Fe作催化剂条件下,苯和溴发生取代反应生成溴苯,同时有HBr生成,溴具有挥发性,所以生成的HBr中含有溴单质;
步骤2:反应结束后,冷却至常温过滤反应液,滤去难溶性固体;
步骤3:滤液用水洗,洗去生成的FeBr3,溴易溶于溴苯中,所以粗溴苯中含有溴单质,溴能和NaOH反应但溴苯和NaOH不反应,用NaOH溶液除去溴苯中的溴,从而得到粗溴苯;
步骤4:向粗溴苯中加入少量无水氯化钙,静置、过滤,氯化钙具有吸水性,作干燥剂;
HBr不能直接排空,且能和NaOH反应,所以用NaOH溶液除去HBr.
(1)在苯和溴的取代反应中,Fe作催化剂;在Fe作催化剂条件下,苯和溴发生取代反应生成溴苯,同时有HBr生成,反应方程式为 +Br2$\stackrel{Fe}{→}$
+Br2$\stackrel{Fe}{→}$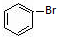 +HBr,故答案为:催化剂;
+HBr,故答案为:催化剂; +Br2$\stackrel{Fe}{→}$
+Br2$\stackrel{Fe}{→}$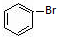 +HBr;
+HBr;
(2)仪器c是冷凝管,冷凝管有冷凝回流作用,提高反应物的利用率,故答案为:冷凝回流;
(3)步骤3中用水洗涤除去可溶性杂质,溴苯中含有易溶于水的杂质溴化铁,所以用水洗涤目的是除去FeBr3;溴能和氢氧化钠反应生成可溶性的钠盐,所以后用NaOH溶液洗涤除去Br2,故答案为:FeBr3;Br2;
(4)分离互溶性液体应该采用蒸馏方法,这几种液体互溶且熔沸点、密度相差不大,应该采用蒸馏方法分离,故答案为:蒸馏.
点评 本题考查溴苯制备实验方案设计,为高频考点,侧重考查实验基本操作、仪器用途、物质的分离和提纯等知识点,明确实验原理是解本题关键,熟悉各仪器的作用,题目难度中等.

 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案| A. | c(Na+)>c(Ac-)>c(OH-)>c(H+) | B. | c(Na+)=c(Ac-)>c(OH-)>c(H+) | ||
| C. | c(Na+)>c(OH-)>c(Ac-)>c(H+) | D. | c(Na+)>c(OH-)>c(H+)>c(Ac-) |

有关性质如下表:
| 物质 | 熔点/℃ | 沸点/℃ | 其他 |
| SiHCl3 | -126.5℃ | 33.0 | 易与水强烈反应,空气中易自然 |
| SiCl4 | -70 | 57.6 | 易水解 |
| HCl | -114.2 | -84.7 |
(2)第②步经冷凝得到的SiHCl3中含有少量SiCl4和HCl,提纯SiHCl3采用的方法是蒸馏;尾气中含有少量SiCl4和HCl,可通过NaOH(碱)溶液除去.
(3)实验室用SiHCl3与过量H2反应制备纯硅的装置如下(热源及夹持装置略去):
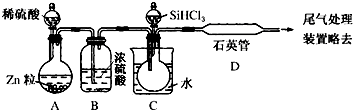
①需要加热的装置有CD(填序号);如无装置B则C中能发生的副反应方程式是SiHCl3+3H2O═H2SiO3+H2↑+3HCl.
②制备实验操作成功的关键是检查实验装置的气密性,控制好反应温度以及实验开始时先通一段时间H2,将装置中的空气排尽;反应一段时间后,装置D中观察到的现象是有固体物质生成(石英管的内壁附有灰黑色晶体).
(4)粗硅中一般含有微量铁、铝、碳、硼、磷、铜等杂质,为鉴定硅中是否含铁,将试样用稀盐酸溶解,取上层清液后加入的最佳试剂是:bd(填写字母代号).
a.碘水 b.氯水 c.NaOH溶液 d.KSCN溶液 e.Na2SO3溶液.
(1)下面为CO2加氢制取低碳醇的热力学数据:
反应Ⅰ:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0 kJ•mol-1
反应Ⅱ:2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(g)△H=-173.6kJ•mol-1
写出由CH3OH(g)合成CH3CH2OH(g)的热化学反应方程式:2CH3OH(g)?CH3CH2OH(g)+H2O(g)△H=-75.6 kJ•mol-1
(2)工业合成甲醇的反应:CO(g)+2H2(g)?CH3OH(g)△H<0.
①该反应在不同温度下的化学平衡常数(K)如下表:
| 温度/℃ | 250 | 350 |
| K | 2.041 | x |
A.0 B.0.012
C.32.081 D.100
②若装置乙为容积固定的密闭容器,不同时间段各物质的浓度如下表:
| c(CO) | c(H2) | c(CH3OH) | |
| 0min | 0.8mol•L-1 | 1.6mol•L-1 | 0 |
| 2min | 0.6mol•L-1 | y | 0.2mol•L-1 |
| 4min | 0.3mol•L-1 | 0.6mol•L-1 | 0.5mol•L-1 |
| 6min | 0.3mol•L-1 | 0.6mol•L-1 | 0.5mol•L-1 |
A.使用催化剂 B.降低温度 C.增加H2的浓度 D.升高温度
(3)全钒液流储能电池(VRB)广泛应用于风能、太阳能发电系统的储能系统,电池反应为VO2++V2++2H+
 VO2++V3++H2O,试推写出放电时正极的电极反应式VO2++2H++e-=VO2++H2O.
VO2++V3++H2O,试推写出放电时正极的电极反应式VO2++2H++e-=VO2++H2O.(4)如图2为某温度下,Fe(OH)3(s)、Mg(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液的pH,金属阳离子浓度变化情况.据图分析:该温度下,溶度积常数的关系为:Ksp[Fe(OH)3]<Ksp[Mg(OH)2](填:>、=、<);如果在新生成的Mg(OH)2浊液中滴入足量的Fe3+,振荡后,白色沉淀会全部转化为红褐色沉淀,原因是浊液中存在溶解平衡:Mg(OH)2
 Mg2++2OH-,当加入Fe3+后与OH-生成更难溶解的Fe(OH)3,使平衡继续向右移动,最后Mg(OH)2全部溶解转化为红棕色的Fe(OH)3.
Mg2++2OH-,当加入Fe3+后与OH-生成更难溶解的Fe(OH)3,使平衡继续向右移动,最后Mg(OH)2全部溶解转化为红棕色的Fe(OH)3.
(1)氮是地球上含量丰富的一种元素,工业上用N2和H2合成NH3.
①已知:N2(g)+3H2(g)?2NH3(g)△H=-92.2kJ•mol-1
N2(g)+O2(g)?2NO(g)△H=+180kJ•mol-1
H2(g)+$\frac{1}{2}$O2(g)?H2O(l)△H=-285.8kJ•mol-1
则4NH3(g)+5O2(g)═4NO(g)+6H2O(l)△H=-1170.4kJ•mol-1.
②现将1mol N2(g)、3mol H2(g)充入一容积为2L的密闭容器中,在500℃下进行反应,10min时达到平衡,下列说法中正确的是C.
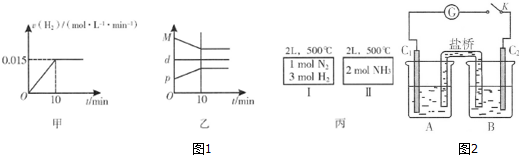
A.图1甲为用H2表示的反应速率变化曲线
B.图1乙表示反应过程中,混合气体平均相对分子质量为M,混合气体密度为d,混合气体压强为p的变化情况
C.图1丙的两个容器中分别发生反应:N2(g)+3H2(g)?2NH3(g)、2NH3(g)?N2(g)+3H2(g).达到化学平衡时,相同组分的浓度相等且两个反应的平衡常数互为倒数
(2)反应PCl5(g)?PCl3(g)+Cl2(g)△H>0,在2L密闭容器中放人1molPCl5,保持一段时间后达到平衡.反应过程中测定的部分数据见下表:
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
②该温度下,该反应的平衡常数为0.025.
(3)①推断As元素在周期表中的位置是第四周期VA族.
②已知某砷酸盐可发生如下反应:AsO43-+2I-+2H+?AsO33-+I2+H2O.某化学兴趣小组利用该反应原理设计如图2所示装置:C1、C2是石墨电极,A中盛有KI和I2混合溶液,B中盛有Na3AsO4和Na3AsO3的混合溶液,当连接开关K后,A中溶液颜色逐渐变深,灵敏电流计G的指针向右偏转.此时C2上发生的电极反应式是AsO42-+2H++2e-=AsO32-+H2O;一段时间后,当电流计指针回到中间“0”位时,再向B中滴加过量浓NaOH溶液,可观察到电流计指针向左偏(填“不动”、“向左偏”或“向右偏”).
 已知NH3和HCl都能用来作喷泉实验的气体,若在同温同压下用等体积烧瓶一个收集满NH3,另一个收集HCl和N2的混合气体,如图所示,喷泉实验停止后,两个烧瓶内溶液的溶质的物质的量浓度(c)和溶质的质量分数(w)关系是( )
已知NH3和HCl都能用来作喷泉实验的气体,若在同温同压下用等体积烧瓶一个收集满NH3,另一个收集HCl和N2的混合气体,如图所示,喷泉实验停止后,两个烧瓶内溶液的溶质的物质的量浓度(c)和溶质的质量分数(w)关系是( )| A. | c和w都不同 | B. | c和w都相同 | C. | c相同,w不同 | D. | w相同,c不同 |
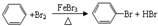 ,该有机反应的类型为取代反应.
,该有机反应的类型为取代反应. 按要求完成下列问题.
按要求完成下列问题.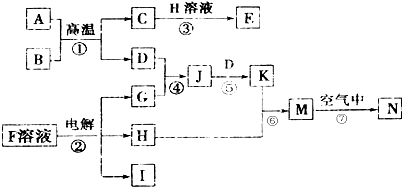
 ,N的化学式为Fe(OH)3.
,N的化学式为Fe(OH)3.