题目内容
已知:A、B、C、D、E为四种短周期元素,它们的核电荷数大小顺序是A<B<D<C;A与B可形成共价化合物AB2,每个AB2分子中含有22个电子;D元素与A元素为同主族元素,C元素原子的最外层电子数比次外层少1个.试回答下列问题:
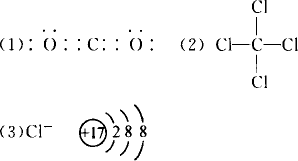
(1)写出AB2的电子式:________.
(2)写出A与C形成的共价化合物的结构式:________.
(3)写出C-的结构示意图:________.
(4)D元素和B元素也能形成DB2型共价化合物,但它与AB2相比,在物理性质上有巨大反差.请你从结构上给予合理的解释:________.
答案:
解析:
解析:
|
(4)因为SiO2是原子晶体,原子间通过很强的共价键结合起来;而CO2是分子晶体,分子间通过较弱的分子间作用力结合起来 |

练习册系列答案
相关题目
 (2011?新余二模)化学--选修物质结构与性质
(2011?新余二模)化学--选修物质结构与性质
 已知:A、B、C、D、E、F、X为周期表中前四周期的七种元素,它们的原子序数依次增大.A是周期表中原子半径最小的元素;B的基态原子有3个不同的能级,各能级中电子数相等;D的基态原子2p能级上的未成对电子数与B原子的相同;D2-离子与E2+离子具有相同的稳定电子层结构;F有“生物金属”之称,F4+离子和氩原子的核外电子排布相同;X的基态原子的价电子排布式为3d84s2.
已知:A、B、C、D、E、F、X为周期表中前四周期的七种元素,它们的原子序数依次增大.A是周期表中原子半径最小的元素;B的基态原子有3个不同的能级,各能级中电子数相等;D的基态原子2p能级上的未成对电子数与B原子的相同;D2-离子与E2+离子具有相同的稳定电子层结构;F有“生物金属”之称,F4+离子和氩原子的核外电子排布相同;X的基态原子的价电子排布式为3d84s2.
 已知单质A、B、C、D有如下的反应关系.其中A 在B中燃烧时,火焰呈苍白色; C在B中燃烧时生成棕黄色的烟,E的水溶液呈蓝绿色,G是一种黑色固体.
已知单质A、B、C、D有如下的反应关系.其中A 在B中燃烧时,火焰呈苍白色; C在B中燃烧时生成棕黄色的烟,E的水溶液呈蓝绿色,G是一种黑色固体.