题目内容
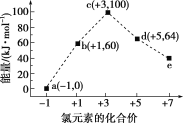
【题目】一定条件下,在水溶液中1 mol ClOx-(x=0,1,2,3,4)的能量(kJ)相对大小如图所示,下列有关说法正确的是( )
A.e是ClO3-
B.b→a+c反应的活化能为60 kJ·mol-1
C.a、b、c、d、e中c最稳定
D.b→a+d反应的热化学方程式为3ClO-(aq)=2Cl-(aq)+ClO3-(aq) ΔH=-116 kJ·mol-1
【答案】D
【解析】
从图中可知,各微粒中氯元素的化合价:a为-1价,b为+1价,c为+3价,d为+5价,e为+7价。根据氧化还原反应写出b→a+c和b→a+d的离子反应方程式。
A选项,根据图可知e对应的价态为+7价,因此该离子为ClO4-,故A错误;
B选项,b→a+c即2ClO-(aq)= Cl-(aq)+ClO2-(aq) ΔH=(100 kJ·mol-1+0 kJ·mol-1)2×60 kJ·mol-1 = 20 kJ·mol-1,该反应为放热反应,但无法知道该反应的活化能,故B错误;
C选项,根据能量越低越稳定,a、b、c、d、e中a能量最低,所以a最稳定,故C错误;
D选项,b→a+d反应的热化学方程式为3ClO-(aq)=2Cl-(aq)+ClO3-(aq) ΔH=(64kJ/mol+2×0kJ/mol)3×60kJ/mol=116kJ/mol,为放热反应,反应物的键能之和小于生成物的键能之和,故D正确;
综上所述,答案为D。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目