题目内容
【题目】下图是一个化学过程的示意图。
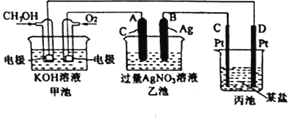
(1)C(Pt)电极的名称是__________。
(2)写出通入O2的电极上的电极反应式_______________________。
(3)写出通入CH3OH的电极上的电极反应式________________________。
(4)若丙池是电解饱和食盐水溶液,则阳极的电极反应为________________________。
(5)写出乙池中反应的化学方程式________________________。
(6)当乙池中B(Ag)极的质量增加5.40 g时,甲池中理论上消耗O2_________mL(标准状况下);若丙池中饱和食盐水溶液的体枳为500 mL,电解后,溶液的pH=________。(25℃,假设电解前后溶液的体积无变化)。
【答案】 阳极 O2+2H2O+4e-=4OH- CH3OH+8OH--6e-=CO32-+6H2O 2Cl--2e-=Cl2↑ 2H2O+4AgNO3![]() 4Ag+O2↑+4HNO3 280 13
4Ag+O2↑+4HNO3 280 13
【解析】燃料电池中,通入燃料的电极为负极,电极反应为CH3OH+8OH--6e-=CO32-+6H2O ,通入氧化剂的电极为正极,正极反应为O2+2H2O+4e-=4OH-;乙池、丙池是电解池,与电源正极相连的是阳极,与电源负极相连的是阴极,则A是阳极、B是阴极,乙池中阳极、阴极电极反应分别为![]() 、
、![]() ,丙池中C是阳极,D是阴极,电解质溶液是氯化钠溶液,氢离子在阴极放电,氯离子在阳极放电。
,丙池中C是阳极,D是阴极,电解质溶液是氯化钠溶液,氢离子在阴极放电,氯离子在阳极放电。
(1)通入氧气的电极是正极,C(Pt)电极的名称是阳极;正确答案:阳极。
(2)通入氧气的电极上的电极反应式是O2+2H2O+4e-=4OH-;正确答案:O2+2H2O+4e-=4OH-。
(3)燃料电池中,通入燃料的电极为负极,甲醇分子失电子在碱性环境下生成碳酸根离子,电极反应为:CH3OH+8OH--6e-=CO32-+6H2O;正确CH3OH+8OH--6e-=CO32-+6H2O。
(4)丙池中C是阳极,D是阴极,电解质溶液是氯化钠溶液,氯离子在阳极失电子产生氯气,电极反应为:2Cl--2e-=Cl2↑;正确答案:2Cl--2e-=Cl2↑。
(5)乙池中A是阳极、B是阴极,阳极水电离出的氢氧根失电子产生氧气,阴极银离子得电子产生单质银,属于放氧生酸型,电解反应的化学方程式为:2H2O+4AgNO3![]() 4Ag+O2↑+4HNO3 ;正确答案:2H2O+4AgNO3
4Ag+O2↑+4HNO3 ;正确答案:2H2O+4AgNO3![]() 4Ag+O2↑+4HNO3。
4Ag+O2↑+4HNO3。
(6)当乙池中B(Ag)极的质量增加5.40 g时,根据![]() ,转移电子为
,转移电子为![]() ,根据甲池中O2+2H2O+4e-=4OH-,标况下,甲池中理论上消耗氧气的体积
,根据甲池中O2+2H2O+4e-=4OH-,标况下,甲池中理论上消耗氧气的体积![]() ,产生氢氧根离子的物质的量
,产生氢氧根离子的物质的量![]() ,
,![]() ,则溶液
,则溶液![]() ;正确答案:280; 13。
;正确答案:280; 13。