题目内容
【题目】人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格.
(1)铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4═2PbSO4+2H2O.正极电极反应式为 .
(2)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu═2FeCl2+CuCl2 , 若将此反应设计成原电池,则负极所用电极材料为 , 当线路中转移0.4mol电子时,则被腐蚀铜的质量为g.
(3)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为 .
A.铝片、铜片
B.铜片、铝片
C.铝片、铝片
(4)如图是一种新型燃料电池,以CO为燃料,一定比例的Li2CO3和Na2CO3的熔融混合物为电解质,A极为电源(填“正”或“负”)极,写出A极的电极反应式: . 
【答案】
(1)PbO2+4H++SO42﹣+2e﹣═PbSO4+2H2O
(2)Cu;12.8
(3)B
(4)负极;CO﹣2e﹣+CO32﹣=2CO2
【解析】解:(1)放电时,正极上PbO2得电子,正极反应式为PbO2+4H++SO42﹣+2e﹣═PbSO4+2H2O,所以答案是:PbO2+4H++SO42﹣+2e﹣═PbSO4+2H2O;(2)该电池反应中,铜失电子发生氧化反应,作负极;负极反应式为Cu﹣2e﹣=Cu2+ , 则当线路中转移0.4mol电子时,反应的Cu为0.2mol,其质量为12.8g,所以答案是:Cu;12.8;(3)铝片和铜片插入浓HNO3溶液中,金属铝会钝化,金属铜和浓硝酸之间会发生自发的氧化还原反应,此时金属铜时负极,金属铝是正极; 插入稀NaOH溶液中,金属铜和它不反应,金属铝能和氢氧化钠发生自发的氧化还原反应,此时金属铝是负极,金属铜是正极,所以答案是:B;(4)CO具有还原性,在负极上发生氧化反应生成CO2 , 则A为燃料电池的负极,电解质为Li2CO3和Na2CO3的熔融混合物,则电极反应式为:CO﹣2e﹣+CO32﹣═2CO2 , 所以答案是:负;CO﹣2e﹣+CO32﹣=2CO2 .

【题目】在锌与盐酸反应的实验中,一个学生得到的结果如下表所示:
编号 | 锌的质量/g | 锌的形状 | 温度/℃ | 完全溶解 |
A | 2 | 薄片 | 5 | 400 |
B | 2 | 薄片 | 15 | 200 |
C | 2 | 薄片 | 25 | 100 |
D | 2 | 薄片 | 35 | t1 |
E | 2 | 细小颗粒 | 15 | t2 |
F | 2 | 粉末 | 15 | t3 |
G | 2 | 薄片(含少量杂质Cu) | 35 | t4 |
(1)t1=s,画出以时间对温度的曲线图(纵轴表示时间,横轴表示温度). 
(2)利用所画的曲线图,总结并得出的关于温度影响反应速率的结论是;
(3)t1t4(填“>”或“<”),原因是 . t2t3(填“>”或“<”),原因是;
(4)单位时间内消耗锌的质量mB、mE、mF从大到小的顺序为 .
【题目】重金属元素铬的毒性较大,含铬废水需经处理达标后才能排放。
(Ⅰ)某工业废水中主要含有Cr3+,同时还含有少量的Fe2+、Fe3+、Al3+、Ca2+和Mg2+等,且酸性较强。为回收利用,通常采用如下流程处理:
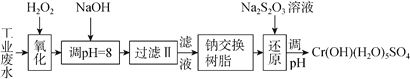
注:部分阳离子常温下以氢氧化物形式完全沉淀时溶液的pH见下表。
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Mg(OH)2 | Al(OH)3 | Cr(OH)3 |
pH | 3.7 | 9.6 | 11.1 | 8 | 9(>9溶解) |
(1)氧化过程中可代替H2O2加入的试剂是________(填序号)。
A.Na2O2 B.HNO3 C.FeCl3 D.KMnO4
(2)加入NaOH溶液调整溶液pH=8时,除去的离子是___(填序号);已知钠离子交换树脂的原理:Mn++nNaRMRn+nNa+,此步操作被交换除去的杂质离子___(填序号)。
A.Fe3+ B.Al3+ C.Ca2+ D.Mg2+
(3)在还原过程中,每消耗172.8gCr2O72- 转移4.8mole-,则还原过程中该反应离子方程式为____。(已知在氧化过程中Cr3+转化为Cr2O72- )
(Ⅱ)酸性条件下,铬元素主要以Cr2O72-形式存在,工业上常用电解法处理含Cr2O72-的废水。实验室利用如图装置模拟处理该废水,阳极反应是Fe-2e-![]() Fe2+,阴极反应式是2H++2e-
Fe2+,阴极反应式是2H++2e-![]() H2↑。
H2↑。
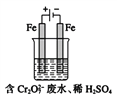
(1)电解时能否用Cu电极来代替Fe电极?______(填“能”或“不能”),理由是_____。
(2)电解时阳极附近溶液中转化为Cr3+的离子方程式为___________________。
(3)上述反应得到的金属阳离子在阴极区可沉淀完全,从其对水的电离平衡影响角度解释其原因______________________。
(4)若溶液中初始含有0.1mol Cr2O72-,则生成的阳离子全部转化成沉淀的质量是_______g。


