题目内容
⑴配平反应器中发生的反应方程式:
I2 + KIO3 + H2O="=" KH(IO3)2 + KCl + Cl2↑
⑵步骤②中,用硝酸而不用HI,其原因可能是
⑶步骤③要保持溶液微沸1小时,以完全排出氯气,排出氯气的原因为
⑷合成实验中涉及两次过滤,在实验室进行过滤实验时,用到的玻璃仪器有
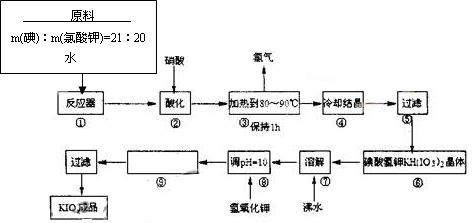
⑸用氢氧化钾调节溶液的PH值,发生的反应方程式为:
⑹参照碘酸钾溶解度曲线,步骤得到碘酸钾晶体,你建议的方法是
| 温度 | 0 | 10 | 20 | 40 | 60 | 80 |
| KIO3g/100g水 | 4.60 | 6.27 | 8.08 | 12.6 | 18.3 | 24.8 |
(每空2分)(1)6,11,3=6,5,3;(2)HI具有还原性能将已生成的碘酸氢钾还原;(3)反应产生氯气跟KOH反应生成KClO,KClO能将KIO3氧化成KIO4,从而不能得到KIO3。(4)漏斗、烧杯、玻璃棒;(5)KH(IO3)2 +KOH==2KIO3+H2O;(6)蒸发结晶。
该题以KIO3制备实验为载体,考查了氧化还原反应及其方程式配平,过滤实验的仪器、物质的分离方法等。图、表结合,考查学生的阅读理解能力。(1)略(2)HI有较强还原性,IO3-有较强氧化性,二者发生反应:5I-+IO3-+6H+==3I2+3H2O,所以不能用HI酸化;(3)因为ClO-有强氧化性能将KIO3氧化成KIO4,故在加KOH之前要予以排除。(4)、(5)略(6)由表中数据可知KIO3在常温下的溶解度较小,又KIO3在650℃即分解,故最好采用蒸发浓缩溶液,让KIO3结晶析出再行过滤分离的方法。

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案
相关题目
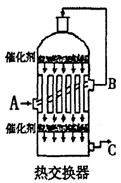
 2ZnO+2SO2 2C+O2
2ZnO+2SO2 2C+O2