题目内容
【题目】下列物质的制备与工业生产相符的是
①NH3 ![]() NO
NO ![]() HNO3
HNO3
②浓HCl ![]() Cl2
Cl2 ![]() 漂白粉
漂白粉
③MgCl2(aq) ![]() 无水MgCl2
无水MgCl2 ![]() Mg
Mg
④饱和NaCl(aq) ![]() NaHCO3
NaHCO3 ![]() Na2CO3
Na2CO3
⑤铝土矿![]() NaAlO2溶液
NaAlO2溶液![]() Al(OH)3
Al(OH)3![]() Al2O3
Al2O3 ![]() Al
Al
A.①④⑤ B.①③⑤ C.②③④ D.②④⑤
【答案】A
【解析】
试题分析:氨气发生催化氧化生成NO和H2O,生成的NO与氧气、水反应可以转化为硝酸,①正确;实验室制取氯气用二氧化锰氧化浓盐酸,而工业上利用电解饱和食盐水制备氯气,②不正确;氯化镁溶液中存在水解平衡MgCl2+2H2O![]() Mg(OH)2+2HCl,水解吸热,加热促进水解。且生成的氯化氢极易挥发,因此最终得到氢氧化镁固体,得不到氯化镁,③不正确;④属于侯氏制碱法原理,正确;铝土矿中含有两性氧化物氧化铝,能溶解在氢氧化钠溶液中生成偏铝酸钠,偏铝酸钠吸收CO2即转化为氢氧化铝沉淀。氢氧化铝分解得到氧化铝。电解熔融的氧化铝即可冶炼金属铝,⑤正确,所以答案选A。
Mg(OH)2+2HCl,水解吸热,加热促进水解。且生成的氯化氢极易挥发,因此最终得到氢氧化镁固体,得不到氯化镁,③不正确;④属于侯氏制碱法原理,正确;铝土矿中含有两性氧化物氧化铝,能溶解在氢氧化钠溶液中生成偏铝酸钠,偏铝酸钠吸收CO2即转化为氢氧化铝沉淀。氢氧化铝分解得到氧化铝。电解熔融的氧化铝即可冶炼金属铝,⑤正确,所以答案选A。

 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案【题目】汽车尾气中的主要污染物是NO和CO。为减轻大气污染,人们提出通过以下反应来处理汽车尾气:
(1)2NO(g)+2CO(g)![]() 2CO2(g)+N2(g)△H=﹣746.5kJmol-1(条件为使用催化剂)
2CO2(g)+N2(g)△H=﹣746.5kJmol-1(条件为使用催化剂)
已知:2C(s)+O2(g)![]() 2CO(g)△H=﹣221.0kJmol-1
2CO(g)△H=﹣221.0kJmol-1
C(s)+O2(g)![]() CO2(g)△H=﹣393.5kJmol-1
CO2(g)△H=﹣393.5kJmol-1
则N2(g)+O2(g)=2NO(g) △H = kJmol-1。
(2)T ℃下,在一容积不变的密闭容器中,通入一定量的NO和CO,用气体传感器测得不同时间NO和CO的浓度如下表
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)/10-4 mol/L | 10.0 | 4.50 | c1 | 1.50 | 1.00 | 1.00 |
c(CO)/10-3 mol/L | 3.60 | 3.05 | c2 | 2.75 | 2.70 | 2.70 |
则c2合理的数值为 (填字母标号)。
A.4.20 B.4.00 C.2.95 D.2.80
(3)将不同物质的量的H2O(g)和CO(g)分别通入体积为2 L的恒容密闭容器中,进行反应:H2O(g)+CO(g)![]() CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
H2O | CO | CO | H2 | |||
i | 650 | 2 | 4 | 2.4 | 1.6 | 5 |
ii | 900 | 1 | 2 | 1.6 | 0.4 | 3 |
iii | 900 | a | b | c | d | t |
若a=2,b=1,则c= ,达平衡时实验组ii中H2O(g)和实验组iii中CO的转化率的关系为αii(H2O) αiii(CO)(填“<”、“>”或“=”)。
(4)二甲醚是清洁能源,用CO在催化剂存在下制备二甲醚的反应原理为:2CO(g)+4H2(g)![]() CH3OCH3(g)+H2O(g),已知一定条件下,该反应中CO的平衡转化率随温度、投料比
CH3OCH3(g)+H2O(g),已知一定条件下,该反应中CO的平衡转化率随温度、投料比![]() 的变化曲线如图1所示。
的变化曲线如图1所示。
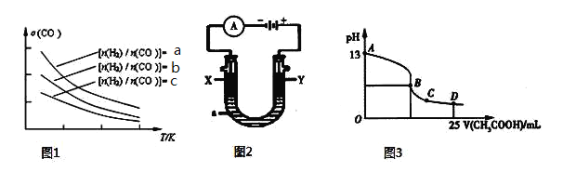
① a、b、c按从大到小的顺序排序为 。
② 根据图象可以判断该反应为 反应(填吸热或放热)。
(5)CO分析仪的传感器可测定汽车尾气是否符合排放标准,该分析仪的工作原理类似于燃料电池,其中电解质是氧化钇(Y2O3)和氧化锆(ZrO2)晶体,能传导O2-。
① 负极的电极反应式为 。
② 以上述电池为电源,通过导线连接成图2。若X、Y为石墨,a为2 L 0.1 mol/L KCl溶液电解一段时间后,取25 mL 上述电解后的溶液,滴加0.4 mol/L醋酸得到图3曲线(不考虑能量损失和气体溶于水,溶液体积变化忽略不计)。根据图2计算,上述电解过程中消耗一氧化碳的质量为 g。
【题目】已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去),则W、X不可能是
选项 | W |
|
A | 稀硫酸 | NaAlO2溶液 |
B | 稀硝酸 | Fe |
C | CO2 | Ca(OH)2溶液 |
D | Cl2 | Fe |

