题目内容
若NA表示阿伏加德罗常数的数值,下列说法正确的是
| A.1 mol氦气分子中含2NA个氦原子 |
| B.在0℃、101kPa时,22.4L氢气中含有NA个氢原子 |
| C.在标准状况下,22.4L空气中约有NA个气体分子 |
| D.25℃时,l L pH=13的Ba(OH)2溶液中含 Ba2+的数目为0.1NA |
C
解析试题分析:氦元素是0族元素,具有稳定电子层结构,因此氦气分子是单原子分子,则1mol氦气分子含有1mol氦原子,故A错误;0℃、101kPa就是标准状况,由于Vm=22.4L/mol、n=V/Vm,则n(H2)=1mol,氢气分子是双原子分子,则1mol氢气分子含有2mol氢原子,故B错误;混合气体的物质的量也可以用n=V/Vm计算,则空气中各种分子总物质的量为1mol,1mol混合气体含有NA个气体分子,故C正确;25℃时溶液中Kw =10-14, c(H+)=10-pHmol/L,c(OH-)=Kw/ c(H+)=10-1mol/L,由于n=c?V,则n(OH-)= 10-1mol/L×1L=0.1mol,由于Ba(OH)2是强电解质,Ba(OH)2=Ba2++2OH-中各物质的系数之比等于物质的量之比,则n(Ba2+)= n(OH-)/2=0.05mol,故D错误。
考点:考查阿伏加德罗常数,设计物质的组成、气体摩尔体积、水的离子积、溶液的pH、电离方程式、物质的量浓度、体积等。

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案
相关题目
下列有关化学用语表示不正确的是
A.氧的原子结构示意图: |
B.Na2O2的电子式: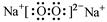 |
| C.HClO的结构式:H-O-Cl |
D.中子数为16的硫离子: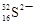 |
用NA表示阿伏加德罗常数的值。下列叙述正确的是
| A.2.24L CH4气体中含有的电子数为NA |
| B.25℃时,1.0L PH=13的Ba(OH)2溶液中含有的OH-数目为0.2NA |
| C.0.1NA个氯气份了溶于水形成1L溶液,所得溶液中c(C1-)=0.1mol·L-1 |
| D.1molCH3COONa和少量CH3COOH溶于水形成的中性溶液中,CH3COO-数目为NA |
下列有关化学用语表示正确的是
A.羧基电子式 |
B.O2-的结构示意图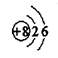 |
C.质子数35,中子数44的溴原子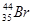 |
D.Al(OH)3在水溶液中的电离方程式H++H2O+AlO2- AI(OH)3 AI(OH)3 Al3++3OH- Al3++3OH- |
设NA为阿伏加德罗常数,下列说法正确的是
| A.标准状况下,5.6 L四氯化碳含有的分子数为0.25NA |
| B.1 mol硫酸钾中阴离子所带电荷数为NA |
| C.标准状况下,22.4 L氯气与足量氢氧化钠溶液反应转移的电子数为NA |
| D.常温下,0.1mol/L的NH4NO3溶液中氮原子数为0.2NA |
NA表示阿伏加德罗常数值。下列说法正确的是
| A.1mol Na2O2与足量CO2充分反应转移的电子数为2NA |
| B.常温下,pH=1的醋酸溶液中,醋酸分子的数目一定大于0.1NA |
| C.向FeI2溶液中通入适量氯气,当有1mol Fe2+被氧化时,总共转移电子的数目为NA |
| D.t℃时,1L pH=6的纯水中,含1×10—6 NA个OH— |
若NA表示阿伏加德罗常数,下列说法正确的是
| A.标准状况下,2.24LCl2与过量的稀NaOH 溶液反应,转移电子总数为0.2NA |
| B.1 mol·L-1 CaCl2溶液含有2NA个Cl- |
| C.在标准状况下,22.4L空气中约有NA个气体分子 |
| D.25℃时,l L pH=13的Ba(OH)2溶液中含 Ba2+的数目为0.1NA |
设NA为阿伏加德罗常数的数值,下列说法正确的是
A.已知N2(g)+3H2(g)  2NH3(g) △H=-92.4kJ/mol,在该反应中,当有3NA个电子转移时,上述热化学方程式的焓变变为:△H=-46.2kJ/mol 2NH3(g) △H=-92.4kJ/mol,在该反应中,当有3NA个电子转移时,上述热化学方程式的焓变变为:△H=-46.2kJ/mol |
| B.标准状况下,22.4L空气含有的气体分子总数为NA |
| C.1L0.1mol/L的CH3COOH溶液中含有CH3COOˉ为0.1NA |
| D.1molFe与足量的稀硝酸充分反应,转移的电子数目为2NA |
已知气体的摩尔质量越小,扩散速度越快。如图所示为气体扩散速度的实验,两种气体扩散相遇时形成白色烟环。下列关于甲、乙的判断正确的是
| A.甲是浓氨水,乙是浓硫酸 |
| B.甲是浓盐酸,乙是浓氨水 |
| C.甲是浓氨水,乙是浓盐酸 |
| D.甲是浓硝酸,乙是浓氨水 |