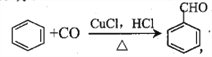题目内容
【题目】如图甲池和乙池中的四个电极都是铂电极,乙池溶液分层,上层溶液为盐溶液,呈中性。请根据图示判断下列有关说法正确的是:( )
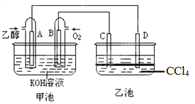
A. 甲池的电解池,乙池是原电池
B. 通入乙醇的铂电极反应式为C2H5OH+16OH-+12e-=2CO32-+11H2O
C. 反应一段时间后,两池溶液的pH均未变化
D. 假如乙池中加入NaI溶液,则在乙池反应过程中,可以观察到C电极周围的溶液呈现棕黄色,反应完毕后,用玻璃棒搅拌溶液,则下层溶液呈现紫红色,上层接近无色
【答案】D
【解析】由图可知甲池是乙醇燃料电池,是原电池,乙池则是电解池,故A错误;在KOH做电解液的条件下,乙醇燃料电池的总反应式为C2H5OH+3O2+4KOH=2K2CO3+5H2O,通入乙醇的电极为负极,负极反应式是C2H5OH+16OH--12e-=2CO32-+11H2O,故B错误;乙醇燃料电池的总反应式为C2H5OH+3O2+4KOH=2K2CO3+5H2O,放电时消耗KOH,溶液的pH减小,故C错误;C与原电池正极相连,是电解池的阳极,I-放电,生成I2,溶液呈黄色,被CCl4萃取后,下层为有机层显紫色,上层为水层呈无色,故D正确。

 口算能手系列答案
口算能手系列答案【题目】废旧电池若不进行回收利用,将对水体产生严重污染。某兴趣小组对废旧镍电池正极材料[由Ni(OH)2、碳粉、Fe2O3等涂覆在铝箔上制成]进行回收研究,设计实验流程如下图所示:
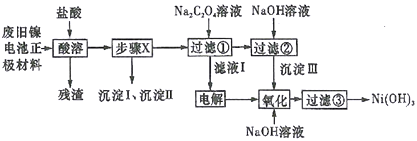
已知:①NiCl2易溶于水,Fe3+不能氧化Ni2+,Cl2能氧化Ni2+为Ni3+;
②NiO+2HCl=NiCl2+H2O;
③Fe3+、Al3+、Ni3+以氢氧化物形式沉淀时溶液的pH如下表所示:
离子 | Fe3+ | Al3+ | Ni2+ |
开始沉淀时的pH | 1.5 | 3.5 | 7.0 |
完全沉淀时的pH | 3.2 | 4.8 | 9.0 |
④Ksp[Ni(OH)2]=5.0×10-16,Ksp(NiC2O4)=4.0×10-10。
请回答下列问题:
(1)酸溶后所留残渣的主要成份__________(填物质名称)。
(2)步骤X的操作为用NiO调节溶液pH,首先析出的沉淀Ⅰ是__________(填化学式),调节过程中pH不能低于___________。
(3)已知溶解度:NiC2O4>NiC2O4·H2O>NiC2O4·2H2O,则加入Na2C2O4溶液后析出的沉淀是__________。
(4)写出生成沉淀Ⅲ的离子方程式__________,该反应的平衡常数为__________。
(5)用化学反应方程式表示沉淀Ⅲ转化为Ni(OH)3________________________。
(6)过滤③后如何检验Ni(OH)3已洗涤干净____________________________。