题目内容
9.一种三室微生物燃料电池可用于污水净化、海水淡化,其工作原理如图所示.以下说法不正确的是( )
| A. | X气体为CO2 | |
| B. | 处理后的含硝酸根废水pH降低 | |
| C. | 中间室中的Cl-移向左室 | |
| D. | 电路中每通过1mol电子,产生标准状况下氮气的体积为2.24L |
分析 该原电池中,硝酸根离子得电子发生还原反应,则右边装置中电极是正极,电极反应式为2NO3-+10e-+12H+=N2↑+6H2O,左边装置电极是负极,负极上有机物失电子发生氧化反应生成X,有机物在厌氧菌作用下生成二氧化碳,据此分析解答.
解答 解:该原电池中,硝酸根离子得电子发生还原反应,则右边装置中电极是正极,电极反应式为2NO3-+10e-+12H+=N2↑+6H2O,左边装置电极是负极,负极上有机物失电子发生氧化反应生成X,有机物在厌氧菌作用下生成二氧化碳,
A.有机物在厌氧菌作用下生成二氧化碳,所以X气体为CO2,故A正确;
B.正极电极反应式为2NO3-+10e-+12H+=N2↑+6H2O,氢离子参加反应导致溶液酸性减小,溶液的pH增大,故B错误;
C.放电时,电解质溶液中阴离子Cl-移向负极室左室,故C正确;
D.根据2NO3-+10e-+12H+=N2↑+6H2O知,电路中每通过1 mol电子,产生标准状况下氮气的体积=$\frac{1mol}{10}$×22.4L/mol=2.24L,故D正确;
故选B.
点评 本题考查化学电源新型电池,侧重考查学生获取信息、分析推断能力,根据N元素化合价变化确定正负极,难点是电极反应式的书写,且原电池和电解池原理是高考高频点,要熟练掌握.

练习册系列答案
相关题目
19.如图所示2个甲分子反应生成1个丙分子和3个乙分子,下列判断不正确的是( )


| A. | 1个乙分子中含有2个A原子 | B. | 摩尔质量关系为:2M (甲)=M (乙)+M (丙) | ||
| C. | 该反应一定属于氧化还原反应 | D. | 该反应类型是分解反应 |
20.H、C、N、O、Na、Al、S、Cl Si是常见的元素
(1)C元素位于元素周期表的位置第二周期,第IVA族;C元素的一种同位素可以测定文物年代,这种同位素的符号为14C.
(2)用“>”、“<”或“=”填空
(3)这些元素中属于第三周期元素的是Na、Al、S、Cl、Si
(4)在(3)中元素的非金属性由强到弱的顺序为Cl>S>Si,能证明其递变规律的事实是CD(填字母)
A.氧化物对应水化物的酸性 B.气态氢化物的沸点
C.单质与氢气反应的难易程度 D.氢化物的稳定性
(5)H、C、N、O、Na、Cl 三种元素间可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式: .
.
(1)C元素位于元素周期表的位置第二周期,第IVA族;C元素的一种同位素可以测定文物年代,这种同位素的符号为14C.
(2)用“>”、“<”或“=”填空
| 离子半径 | 酸性 | 还原性 | 得电子能力 |
| N3-> Al3+ | H2SO4< HClO4 | O2-< S2- | 35Cl= 37Cl |
(4)在(3)中元素的非金属性由强到弱的顺序为Cl>S>Si,能证明其递变规律的事实是CD(填字母)
A.氧化物对应水化物的酸性 B.气态氢化物的沸点
C.单质与氢气反应的难易程度 D.氢化物的稳定性
(5)H、C、N、O、Na、Cl 三种元素间可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:
 .
.
17.用一定体积、一定浓度的盐酸跟过量的锌反应制取一定体积的氢气,为了提高化学反应速率而又不影响生成氢气的体积,下列措施中合理的是( )
| A. | 加少量稀硫酸 | B. | 加热 | C. | 加蒸馏水 | D. | 加少量蓝矾 |
14.X、Y、M、Z四种短周期主族元素的原子半径依次减小,X、Y、Z的电子层数之和为5,X元素原子的最外层电子数是它的电子层数的2倍,Y元素原子的最外层电子数是X和Z两元素原子最外层电子数的总和,M是地壳中含量最多的元素.下列说法不正确的是( )
| A. | 化合物YZ3极易溶解于水 | |
| B. | Z与M可以形成共价化合物 | |
| C. | 12g14X中含有质子的物质的量为6mol | |
| D. | 由上述四种元素组成的离子化合物受热易分解 |
1.下列微粒中,电子数目最多的是( )
| A. | H2O | B. | NH3 | C. | Na+ | D. | Al |
4. 通常人们把拆开1mol 某化学键所吸收的能量看成该化学键的键能.键能的大小可用于估算化学反应的反应热(△H).
通常人们把拆开1mol 某化学键所吸收的能量看成该化学键的键能.键能的大小可用于估算化学反应的反应热(△H).
(1)按要求完成填空
①2HCl(g)=H2(g)+Cl2(g)△H=+183kJ/mol;
②N2(g)+3H2(g)=2NH3(g)△H=-92kJ/mol
则N-H键的键能是391kJ/mol
(2)1mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式为:
NO2(g)+CO(g)=CO2(g)+NO(g)△H=-234 kJ•mol-1
(3)已知:
2Al(s)+$\frac{3}{2}$O2(g)═Al2O3(s)△H=-1 644.3kJ•mol-1
2Fe(s)+$\frac{3}{2}$O2(g)═Fe2O3(s)△H=-815.88kJ•mol-1
试写出铝粉与氧化铁粉末发生铝热反应的热化学方程2Al(s)+Fe2O3(s)═Al2O3(s)+2Fe(s)△H=-828.42kJmol-1.
 通常人们把拆开1mol 某化学键所吸收的能量看成该化学键的键能.键能的大小可用于估算化学反应的反应热(△H).
通常人们把拆开1mol 某化学键所吸收的能量看成该化学键的键能.键能的大小可用于估算化学反应的反应热(△H).| 化学键 | Cl-Cl | H-H | H-Cl | N≡N |
| 键能/kJ•mol | 243 | 436 | 431 | 946 |
①2HCl(g)=H2(g)+Cl2(g)△H=+183kJ/mol;
②N2(g)+3H2(g)=2NH3(g)△H=-92kJ/mol
则N-H键的键能是391kJ/mol
(2)1mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式为:
NO2(g)+CO(g)=CO2(g)+NO(g)△H=-234 kJ•mol-1
(3)已知:
2Al(s)+$\frac{3}{2}$O2(g)═Al2O3(s)△H=-1 644.3kJ•mol-1
2Fe(s)+$\frac{3}{2}$O2(g)═Fe2O3(s)△H=-815.88kJ•mol-1
试写出铝粉与氧化铁粉末发生铝热反应的热化学方程2Al(s)+Fe2O3(s)═Al2O3(s)+2Fe(s)△H=-828.42kJmol-1.
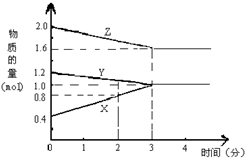 某温度时,在2L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化的曲线如图所示.由图中数据分析:
某温度时,在2L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化的曲线如图所示.由图中数据分析: