题目内容
【题目】已知反应:①101 kPa时,2C(s)+O2(g)=2CO(g) ΔH=-221 kJ·mol-1
②稀溶液中,H+(aq)+OH-(aq)=H2O(l)ΔH=-57.3 kJ·mol-1
③H2(g) ![]() O2(g)=H2O(g)ΔH=-241.8 kJ·mol-1
O2(g)=H2O(g)ΔH=-241.8 kJ·mol-1
④H2O(g)=H2O(l)ΔH=-44.0 kJ·mol-1
下列结论正确的是( )
A.碳的燃烧热大于110.5 kJ·mol-1
B.浓硫酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量
C.氢气的燃烧热为241.8 kJ·mol-1
D.2H2(g)+O2(g)=2H2O(l)的反应热为ΔH=+571.6 kJ·mol-1
【答案】A
【解析】燃烧热是指1 mol物质燃烧生成稳定氧化物所放出的热量,C完全燃烧的产物是CO2,CO继续燃烧生成CO2放出热量,那么C的燃烧热大于110.5 kJ·mol-1;浓硫酸中的H+与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量,但是浓硫酸的稀释又有热量释放,所以该反应过程放出的热量大于57.3 kJ;根据盖斯定律,③④相加得到热化学方程式H2(g)+![]() O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1,该反应为放热反应,故ΔH的符号为“-”。
O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1,该反应为放热反应,故ΔH的符号为“-”。

【题目】用如图装置来分离CO2和CO混合气体并干燥,图中a、c、d为止水夹,b为分液漏斗活塞,通过Y形管和止水夹分别接两个球胆,现装置内空气已排尽,为使实验成功,甲、乙、丙分别盛放的试剂为()
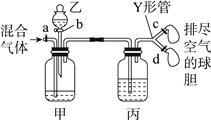
甲 | 乙 | 丙 | |
A | 饱和NaHCO3溶液 | 12 mol·L-1盐酸 | 18.4 mol·L-1 H2SO4 |
B | 饱和Na2CO3溶液 | 2 mol·L-1 H2SO4 | 饱和NaOH溶液 |
C | 饱和NaOH溶液 | 2 mol·L-1 H2SO4 | 18.4 mol·L-1 H2SO4 |
D | 18.4 mol·L-1 H2SO4 | 饱和NaOH溶液 | 18.4 mol·L-1 H2SO4 |
A. A B. B C. C D. D
【题目】下表所列各组物质中,物质之间通过一步反应不能实现右图所示转化的是()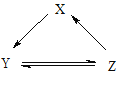
项目 | X | Y | Z |
A | Si | SiO2 | H2SiO3 |
B | Na | NaOH | NaCl |
C | NO | NO2 | HNO3 |
D | NaClO | HClO | Cl2 |
A. A B. B C. C D. D