题目内容
【题目】己知A、B、C是三种常见的固体化合物。焰色反应均显黄色。其中A与C按任意比例混合,溶于足量的水中,得到的溶质只含有一种,并有无色无味的气体D放出。另A、B、C、D之间有如图所示的转化关系(部分物质未写出):
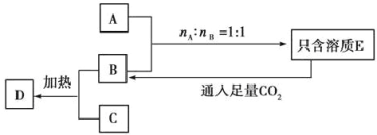
(1)写出下列物质的化学式:
A________、B________、C________。
(2)写出A、B按物质的量之比1:1在密闭容器中加热发生反应的化学方程式:______________________。
(3)写出饱和的E溶液与足量CO2反应的离子方程式:________。
(4)有关铝、铁、铜的说法正确的是________ (填代号)。
a.铝属于主族元素,铁和铜属于过渡元素
b.工业上利用电解法冶炼铝、铁、铜
c.铝、铁、铜对应的氧化物均为碱性氧化物
d.铝、铁、铜常温下都不溶于浓硫酸
【答案】
(1)NaOH;NaHCO3 ;Na2O2
(2)NaOH+NaHCO3![]() Na2CO3+H2O
Na2CO3+H2O
(3)2Na++CO32—+CO2+H2O=2NaHCO3↓
(4)a
【解析】
试题分析:己知A、B、C是三种常见的固体化合物。焰色反应均显黄色,说明含有钠元素。A和B按物质的量1:1反应生成E,E能和二氧化碳反应生成B,说明E为碳酸钠,则B为碳酸氢钠,则A为氢氧化钠; A与C按任意比例混合,溶于足量的水中,得到的溶质只含有一种,并有无色无味的气体D放出,很明显,D不是二氧化碳,则D应该是氧气,C为过氧化钠,结合图像碳酸氢钠受热分解生成二氧化碳和水,二氧化碳与水和过氧化钠均反应放出氧气,满足图像要求。
(1)根据上述分析,A为氢氧化钠;B为碳酸氢钠;C为过氧化钠,故答案为:NaOH;NaHCO3 ;Na2O2 ;
(2)A、B按物质的量之比1:1在密闭容器中加热发生反应的化学方程式为NaOH+NaHCO3![]() Na2CO3+H2O ,故答案为:NaOH+NaHCO3
Na2CO3+H2O ,故答案为:NaOH+NaHCO3![]() Na2CO3+H2O ;
Na2CO3+H2O ;
(3)饱和的碳酸钠溶液与足量CO2反应的离子方程式为2Na++CO32—+CO2+H2O=2NaHCO3↓,故答案为:2Na++CO32—+CO2+H2O=2NaHCO3↓;
(4)a.铝是13号元素,属于ⅢA族元素,铁和铜属于过渡元素,正确;b.工业上利用电解法冶炼铝,用热还原法冶炼铁、铜,错误;c.氧化铝属于两性氧化物,错误;d.铝、铁遇到冷的浓硫酸,在表面形成致密的氧化物薄膜,阻止反应的进一步进行;铜常温下能够与浓硫酸反应,但反应速率很慢,错误;故选a。