题目内容
4.铜及其化合物在工农业生产中都有着广泛应用.(1)火法炼铜首先要焙烧黄铜矿,其反应为:2CuFeS2+2O2=2Cu+2FeS+2SO2,当有1molCu生成,则反应中转移电子6mol.
(2)某种处理火法炼铜中SO2废气的工艺流程如图所示.
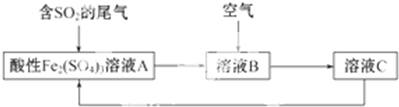
①溶液A中发生的反应为2Fe3++SO2+2H2O=2Fe2++SO42-+4H+.
②由流程图可推知Fe3+、O2、SO42-的氧化性由强到弱的顺序为O2>Fe3+>SO42-.
(3)已知反应:3Cu+2NO3-+xH+=3Cu2++2R+yH2O.则参加反应的Cu和消耗的HNO3物质的量之比为3:8.
分析 (1)2CuFeS2+2O2=2Cu+2FeS+2SO2中,Cu、O元素的化合价降低,S元素的化合价升高;
(2)由工艺流程可知,A中的反应为2Fe3++SO2+2H2O=2Fe2++SO42-+4H+,B中的反应为4Fe2++O2+4H+=4Fe3++2H2O,C中铁离子循环利用,结合氧化还原反应中氧化剂的氧化性大于氧化产物的氧化物分析;
(3)由电荷守恒计算x,由电子守恒计算R中N元素的化合价,从而判断R,然后写出方程式,再计算参加反应的Cu和消耗的HNO3物质的量之比.
解答 解:(1)反应2CuFeS2+2O2=2Cu+2FeS+2SO2中,化合价变化情况为:Cu元素由+2价降低为0价,S元素由-2价升高到+4价,氧气中O元素由0降低为-2价,则每生成2molCu转移电子12mol,则当有1molCu生成,则反应中转移电子为6mol,
故答案为:6;
(2)由工艺流程可知,A中的反应为2Fe3++SO2+2H2O=2Fe2++SO42-+4H+,B中的反应为4Fe2++O2+4H+=4Fe3++2H2O,C中铁离子循环利用,
①由上述分析可知溶液A中的反应为2Fe3++SO2+2H2O=2Fe2++SO42-+4H+,
故答案为:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+;
②A中发生2Fe3++SO2+2H2O=2Fe2++SO42-+4H+,溶液B中发生4Fe2++O2+4H+=4Fe3++2H2O,由氧化剂的氧化性大于氧化产物的氧化性可知氧化性为O2>Fe3+>SO42-,
故答案为:O2>Fe3+>SO42-;
(3)由电荷守恒可得:(-2)+x=2×3,则x=8,设R中氮元素的化合价为a,由得失电子守恒可得:2×(5-a)=2×3,解得a=+2,则R为NO,配平方程式为:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O,所以参加反应的Cu和消耗的HNO3物质的量之比为3:8;
故答案为:3:8.
点评 本题以铜及其化合物为载体考查氧化还原反应的计算,把握发生的反应及反应中元素的化合价变化为解答的关键,侧重分析、计算能力的综合考查,题目难度中等.

 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案| A. | 滤纸 | B. | 烧杯 | C. | 酒精灯 | D. | 玻璃棒 |
| A. | ②④⑤ | B. | ①③⑤ | C. | ①②③ | D. | 全部 |
| A. | 甲、丙中是化学能转变为电能,乙中是电能转变为化学能 | |
| B. | C1、C2分别是阳极、阴极,锌片、铁片上都发生氧化反应 | |
| C. | C1和C3放出的气体相同,铜片和铁片放出的气体也相同 | |
| D. | 甲、乙中溶液的pH逐渐升高,丙中溶液的pH逐渐减小 |
①金刚石和石墨
②CH3CH2Br 和 CH3CH2CH2CH2Cl
③
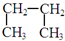 和
和
④CH3CH3 和
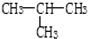
⑤
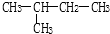 和
和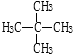
⑥
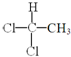 和
和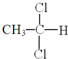
| A. | 化学名为乙酰水杨酸 | B. | 是一种难溶于水的白色晶体 | ||
| C. | 长期大量服用会出现不良反应 | D. | 是一种重要的抗生素即消炎药 |
| A. | 500mL 0.2 mol/L 饱和FeCl3溶液完全转化可制得0.1NA个 Fe(OH)3胶粒 | |
| B. | 分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA | |
| C. | 常温常压下,71g氯气与足量金属钠充分反应,转移的电子数为2 NA | |
| D. | 常温常压下,46g的NO2和N2O4混合气体含有的原子数为3NA |