题目内容
下图是第三周期11~17号元素某些性质变化趋势的柱形图,下列有关说法中正确的是
| A.y轴表示的可能是第一电离能 |
| B.y轴表示的可能是电负性 |
| C.y轴表示的可能是原子半径 |
| D.y轴表示的可能是形成基态离子转移的电子数 |
B
解析试题分析:A、同一周期元素随原子序数依次增大,其第一电离能随着原子序数的增大而增大,如第ⅡA元素的第一电离能大于第ⅢA族的,A错误;B、同一周期元素且原子序数依次增大,其电负性随着原子序数的增大而增大,B正确;C、同一周期元素且原子序数依次增大,其原子半径随着原子序数的增大而减小,C错误;D、同一周期元素随原子序数依次增大,金属失电子数增加,非金属得电子数减少;D错误,选B。
考点:原子结构与元素周期率的关系

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
据报道,美国夏威夷联合天文中心的科学家发现了一种新型氢粒子,这种粒子是由3个氢原子核(只有质子)和2个电子构成。对于这种粒子,下列说法中正确的是( )
| A.是氢的一种新的单质 | B.是氢的一种新的同位素 |
| C.它的组成可用H3表示 | D.它比一个普通H2分子多一个氢原子核 |
元素性质的周期性变化不包括
| A.原子半径 | B.化合价 | C.原子核外电子结构 | D.金属性和非金属性 |
X、Y、Z、W是短周期元素,X元素原子的最外层未达到8电子稳定结构,工业上通过分离液态空气获得其单质;Y元素原子最外电子层上s、p电子数相等;Z元素+2价阳离子的核外电子排布与氖原子相同;W元素原子的M层有1个未成对的p电子。下列有关这些元素性质的说法一定正确的是
| A.X元素的氢化物的水溶液显碱性 |
| B.Z元素的离子半径大于W元素的离子半径 |
| C.Z元素的单质在一定条件下能与X元素的单质反应 |
| D.Y元素最高价氧化物的晶体具有很高的熔点和沸点 |
短周期元素X、Y、Z、W在元素周期表中的相对位置如右图所示,其中X所处的周期序数与族序数相等。下列说法错误的是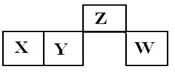
| A.Z的氧化物与W的氧化物的化学键类型相同 |
| B.X、Z的氧化物都能溶于氢氧化钠和稀硫酸溶液中 |
| C.最高价氧化物对应水化物稀溶液的氧化性:W<Z |
| D.Y原子的半径比W原子的半径大 |
短周期主族元素X、Y、Z、W、Q的原子序数依次增大,X的气态氢化物极易溶于Y的氢化物中,常温下,Z的单质能溶于W的最高价氧化物的水化物的稀溶液,却不溶于其浓溶液。下列说法不正确的是
| A.离子半径的大小顺序为Z>W>Q |
| B.元素W的气态氢化物与Y的单质可发生置换反应 |
| C.元素X与Y能在一定条件下发生化合反应,说明Y的非金属性比X强 |
| D.元素Z、W、Q的单质在一定条件下均能和强碱溶液反应 |
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知:
| W | X | |
| | Y | Z |
A.X、Y、Z中最简单氢化物稳定性最弱的是Y
B.Z元素氧化物对应水化物的酸性一定强于Y
C.X元素形成的单核阴离子还原性大于Y
D.Z元素单质在化学反应中只表现氧化性