题目内容
【题目】下列说法不正确的是( )
A.已知冰的熔化热为![]()
![]() ,冰中氢键键能为20
,冰中氢键键能为20![]() ,假设1mol冰中有2mol氢键,且熔化热完全用于破坏冰的氢键,则最多只能破坏冰中
,假设1mol冰中有2mol氢键,且熔化热完全用于破坏冰的氢键,则最多只能破坏冰中![]() 的氢键
的氢键
B.已知:![]() 石墨
石墨![]() ,
,![]()
![]() .
.![]() ,
,![]()
![]() .
.![]() 石墨
石墨![]() ,
,![]()
![]() .则
.则![]() ,
,![]()
![]()
C.实验测得环己烷![]() 、环己烯
、环己烯![]() 和苯
和苯![]() 的标准燃烧热分别为
的标准燃烧热分别为![]()
![]() 、
、![]()
![]() 和
和![]()
![]() ,可以证明在苯分子中不存在独立的碳碳双键
,可以证明在苯分子中不存在独立的碳碳双键
D.已知一定温度下,醋酸溶液的物质的量浓度为c,电离度为![]() ,
,![]() 若加入少量醋酸钠固体,则
若加入少量醋酸钠固体,则![]() 向左移动,
向左移动,![]() 减小,Ka变小
减小,Ka变小
【答案】D
【解析】
![]() 冰是由水分子通过氢键形成的分子晶体,冰的熔化热为
冰是由水分子通过氢键形成的分子晶体,冰的熔化热为![]() ,1mol冰变成
,1mol冰变成![]() 的液态水所需吸收的热量为
的液态水所需吸收的热量为![]() ,全用于打破冰的氢键,冰中氢键键能为
,全用于打破冰的氢键,冰中氢键键能为![]() ,1mol冰中含有2mol氢键,需吸收
,1mol冰中含有2mol氢键,需吸收![]() 的热量,
的热量,![]() 由计算可知,最多只能打破1mol冰中全部氢键的
由计算可知,最多只能打破1mol冰中全部氢键的![]() ,故A正确;
,故A正确;
B.![]() 石墨
石墨![]() ;
;![]()
![]()
![]() ;
;![]()
![]()
![]() 石墨
石墨![]() ;
;![]()
![]()
![]() ;
;![]()
![]()
根据盖斯定律,方程式![]() 可由
可由![]() 可得,
可得, ![]()
![]()
![]()
![]()
![]() ,故B正确;
,故B正确;
C.实验测得环己烷![]() 和环己烯
和环己烯![]() 的标准燃烧热分别为
的标准燃烧热分别为![]() 和
和![]() ,1mol环己烯
,1mol环己烯![]() 与环己烷
与环己烷![]() 相比,形成1mol碳碳双键,能量降低169kJ,假如苯分子中有独立的碳碳双键,苯
相比,形成1mol碳碳双键,能量降低169kJ,假如苯分子中有独立的碳碳双键,苯![]() 与环己烷
与环己烷![]() 相比,形成三个碳碳双键,则能量应降低
相比,形成三个碳碳双键,则能量应降低![]() ,而实际测得苯的燃烧热仅为3265
,而实际测得苯的燃烧热仅为3265![]() ,能量降低了3916
,能量降低了3916![]()
![]() ,远大于
,远大于![]() ,充分说明苯分子不是环己三烯的结构,可以证明在苯分子中不存在独立的碳碳双键,故C正确;
,充分说明苯分子不是环己三烯的结构,可以证明在苯分子中不存在独立的碳碳双键,故C正确;
D.Ka是电离常数,是弱电解质达电离平衡时的平衡常数,在一定温度下,与浓度无关.Ka的计算用溶液中电离出来的各离子浓度乘积与溶液中未电离的电解质分子浓度的比值,一定温度下,醋酸溶液的物质的量浓度为c,电离度为![]() ,
,![]() 醋酸电离出的
醋酸电离出的![]() 和
和![]() 浓度均为
浓度均为![]() ,溶液中未电离的电解质分子浓度为
,溶液中未电离的电解质分子浓度为![]() ,故题中
,故题中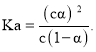 若加入少量醋酸钠固体,
若加入少量醋酸钠固体,![]() 增大了
增大了![]() 的浓度,
的浓度,![]() 向左移动,
向左移动,![]() 减小,但是温度不变,则Ka不变,故D错误。
减小,但是温度不变,则Ka不变,故D错误。
答案:D。

【题目】关于下列各图的叙述不正确的是( )
化学方程式 | 平衡常数K |
F2 + H2 = 2HF | 6.5×1095 |
Cl2 + H2 = 2HCl | 2.6×1033 |
Br2 + H2 = 2HBr | 1.9×1019 |
I2 + H2 = 2HI | 8.7×102 |
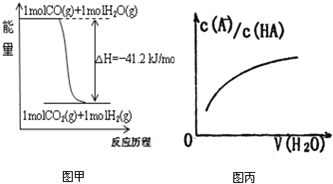
A.已知CO的燃烧热283kJ·mol-1,O2(g) +2 H2(g) = 2H2O(g) ΔH = -483.6 kJ·mol-1,则图甲表示CO和H2O(g)生成CO2和H2的能量变化
B.某温度下,pH =11的NH3H2O和pH =1的盐酸等体积混合后(不考虑混合后溶液体积的变化)恰好完全反应,反应后的溶液中NH4+、NH3H2O与NH3三种微粒的平衡浓度之和为0.05molL-1
C.在常温下,X2(g) 和 H2反应生成HX的平衡常数如表乙所示,仅依据K的变化,就可以说明在相同条件下,平衡时X2(从F2到I2)的转化率逐渐降低,且X2与H2反应的剧烈程度逐渐减弱
D.图丙中曲线表示常温下向弱酸HA的稀溶液中加水稀释过程中,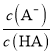 的变化情况
的变化情况