题目内容
3.反应A(g)+3B(g)═2C(g)+2D(g)在四种不同情况下的反应速率分别为①v(A)=0.45mol•L-1•min-1
②v(B)=0.6mol•L-1•s-1
③v(C)=0.4mol•L-1•s-1
④v(D)=0.5mol•L-1•s-1
该反应进行的快慢顺序为( )
| A. | ④>③>②>① | B. | ④<③=②<① | C. | ①>②>③>④ | D. | ④>③=②>① |
分析 不同物质表示的速率之比等于其化学计量数之比,故速率与其化学计量数比值越大,表示的反应速率越快,注意保持单位一致.
解答 解:①v(A)=0.45mol•L-1•min-1=0.0075mol•L-1•s-1,则$\frac{v(A)}{1}$=0.0075mol•L-1•s-1,
②$\frac{v(B)}{3}$=0.2mol•L-1•s-1;
③$\frac{v(C)}{2}$=0.2mol•L-1•s-1;
④$\frac{v(D)}{2}$=0.25mol•L-1•s-1,
故反应速率④>③=②>①,
故选:D.
点评 本题考查化学反应速率快慢比较,难度不大,常利用速率与其化学计量数比值大小比较或转化为同一物质表示的速率比较.

练习册系列答案
 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
13.水是一种廉价而且非常有用的试剂,下列用水就能鉴别的一组物质是( )
| A. | 苯、乙醇、四氯化碳 | B. | 苯、溴苯、四氯化碳 | ||
| C. | 硝基苯、乙醇、四氯化碳 | D. | 硝基苯、乙醇、乙酸 |
14.下列说法不正确的是( )
| A. | 为除去苯中的苯酚,可加入少量溴水溶液,再过滤 | |
| B. | 为除去FeSO4溶液中的Fe2(SO4)3,可加入铁粉,再过滤 | |
| C. | 为除去乙炔气中少量的H2S,可使其通过CuSO4溶液 | |
| D. | 为除去CO2中少量的SO2,可使其通过饱和NaHCO3溶液 |
18.水热法制备直径为1~100nm的颗粒Y(化合物),反应原理为3Fe2++2S2O32-+O2+aOH-═Y+S4O62-+2H2O,下列说法中不正确的是( )
| A. | a=4 | |
| B. | 每有3 mol Fe2+参加反应,反应中转移的电子总数为5 mol | |
| C. | 将Y均匀分散到水中形成的体系具有丁达尔效应 | |
| D. | S2O32-是还原剂 |
8.在硫化钠水溶液中存在着多种离子和分子,下列关系式正确的是( )
| A. | c(S2-)+c(HS-)+c(H2S)+c(H+)=c(OH-) | B. | c(OH-)=c(HS-)+c(H+)+2 c(H2S) | ||
| C. | c(Na+)=c(S2-)+c(HS-)+c(H2S) | D. | c(Na+)+c(H+)=c(S2-)+c(HS-)+c(OH-) |
15.下列关于化学反应与能量变化的关系说法正确的是( )
| A. | 由氢气燃烧放热可知,2mol氢气的能量高于2mol水的能量 | |
| B. | 燃烧天然气做饭时,其能量转化形式只有化学能转化为热能 | |
| C. | 已知碳酸钙分解为吸热反应,则CaO与CO2反应为放热反应 | |
| D. | 根据能量守恒定律分析钠在氯气中燃烧的反应可知,参与反应的钠与氯气的总能量等于生成的氯化钠的总能量 |
12.下列说法不正确的是( )
| A. | 磷酸的摩尔质量(g.mol-1)与6.02×1023个磷酸分子的质量(g)在数值上相等 | |
| B. | 6.02×1023个氮分子和6.02×1023个氢分子的质量比等于14:1 | |
| C. | 32 g氧气所含的原子数目为2NA | |
| D. | 常温常压下,0.5 NA个一氧化碳分子所占体积是11.2 L |
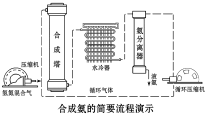 氨在国民经济中占有很重要的地位.现在约有80%的氨用来制造化肥,其余的用作生产其他化工产品的原料.氨氧化法制硝酸是工业上制硝酸的主要方法.
氨在国民经济中占有很重要的地位.现在约有80%的氨用来制造化肥,其余的用作生产其他化工产品的原料.氨氧化法制硝酸是工业上制硝酸的主要方法.