题目内容
2.纳米氧化镁具有特殊的热、光、电、力学和化学等性能,有广泛的应用前景.如图是利用海水制盐的副产品制备纳米氧化镁的流程图.
(1)操作I包括蒸发结晶、过滤.
(2)操作I后得到的母液中镁离子浓度为1.8×10-3 mol•L-1,要使镁离子产生沉淀,溶液的pH最低应为10.(已知:Ksp[Mg(OH)2]=1.8×10-11)
(3)反应I中CO(NH2)2与H20反应生成C02和NH3•H20,还发生另一主要化学反应的离子方程式为Mg2++2NH3•H20=Mg(OH)2↓+2NH4+.
(4)某科研小组研究反应I在378K~398K时的反应时问、反应物的物质的量配比等因素对制备纳米氧化镁产率的影响.请完成以下实验设计表:
| 实验编号 | T/K | 反应时间/h | 反应物的物质的量配比n[CO(NH2)2]:n[MgCl2.6H2O] | 实验目的 |
| ① | 378 | 3 | 3:1 | (I)实验①和③探究反应物的物质的量配比对产率的影响 (II)实验②和④探究温度对产率的影响 (III)实验②和③探究反应时间对产率的影响 |
| ② | 378 | 4 | 4:1 | |
| ③ | 378 | 3 | ||
| ④ | 398 | 4 | 4:1 |

分析 利用海水制盐的副产品制备纳米氧化镁的流程:海水晒盐,过滤得到粗盐、母液,母液中含有氯化镁,加入尿素,反应I中CO(NH2)2与H20反应生成C02和NH3•H20,Mg2++2NH3•H20=Mg(OH)2↓+2NH4+,过滤得到Mg(OH)2沉淀,煅烧Mg(OH)2$\frac{\underline{\;高温\;}}{\;}$MgO+H20,得到氧化镁.
(1)分离固体和液体常用过滤的方法;
(2)结合Ksp[Mg(OH)2]=c(Mg2+)•c2(OH-)=1.8×10-11计算c(OH-),再利用Kw=c(H+)•c2(OH-)计算c(H+),最后根据pH=-lgc(H+)计算;
(3)由工艺流程转化关系可知,反应I中的目的是制备Mg(OH)2,所以反应I中还发生Mg2+与氨水反应生成Mg (OH)2与NH4+;
(4)实验根据控制变量法进行对比试验,研究温度、反应时间、反应物配比对氧化镁产率,分析对比实验的变量不同进行解答;
(5)由图表中数据可知,在378K~398K,纳米MgO的产率随温度升高而升高,在393K之后纳米MgO的产率随温度升高而降低.
解答 解:(1)粗盐含有杂质,海水晒盐,过滤得到粗盐、母液,
故答案为:过滤;
(2)由于Ksp[Mg(OH)2]=c(Mg2+)•c2(OH-)=1.8×10-11,当溶液中c(Mg2+)=10-3mol•L-1,开始沉淀需要OH-浓度为c(OH-)=$\sqrt{\frac{1.8×1{0}^{-11}}{1.8×1{0}^{-3}}}$=10-4 mol•L-1,所以c(H+)=$\frac{1{0}^{-14}}{1{0}^{-4}}$=10-10mol•L-1,pH=-lgc(H+)=-log10-10=10.
故答案为;10;
(3)由工艺流程转化关系可知,加入尿素,反应I中CO(NH2)2与H20反应生成C02和NH3•H20,反应I中的目的是制备Mg(OH)2,所以反应I中还发生Mg2+与氨水反应生成Mg (OH)2与NH4+,反应离子方程式为Mg2++2NH3•H2O=Mg (OH)2↓+2NH4+,
故答案为:Mg2++2NH3•H2O=Mg (OH)2↓+2NH4+;
(4)实验根据控制变量法进行对比试验,研究温度、反应时间、反应物配比对氧化镁产率影响.
(Ⅰ)实验①和③,温度相同,反应时间相同,应研究反应物配比对氧化镁产率的影响,③中反应物配比应为4:1;
(Ⅱ)实验②和④,反应时间相同,反应物配比相同,温度不同,应是探究温度对产率的影响;
(Ⅲ)③中反应物配比应为4:1,实验②和③,温度相同、反应物配比相同,反应时间不同,探究反应时间对产率的影响;
故答案为:
| 实验 编号 | T/K | 反应 时间/h | 反应物的物质的量配比 n[CO(NH2)2]:n[MgCl2•6H2O] | 实验目的 |
| ① | (Ⅰ)反应物的物质的量配比对产率的影响; (Ⅱ)温度对产率的影响; (Ⅲ)③ | |||
| ② | ||||
| ③ | 4:1 | |||
| ④ |
故答案为:其他条件相同时,在378K~398K,纳米MgO的产率随温度升高而升高,之后纳米MgO的产率随温度升高而降低(或其他条件相同时,纳米MgO的产率随温度的升高先升高后降低).
点评 本题考查溶度积计算、盐类水解、对工艺流程的理解与条件的控制、对实验数据图象的分析、移动题目获取信息能力等,题目难度中等,需要学生具备扎实的基础与综合运用知识分析问题、解决问题能力.

 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案| A. | Al | B. | Fe | C. | Cu | D. | Na |

| A. | 上述反应中,△H<0 | |
| B. | c点时,消耗Y和W的速率相等 | |
| C. | 正反应速率:a<b | |
| D. | ac段,升高温度,平衡向正反应方向移动 |
| A. | 16g H2 | B. | 16g S | C. | 24g Mg | D. | 24g C |
| A. |  气体除杂 | B. |  收集氧气 | C. |  稀释溶液 | D. |  滴加溶液 |
| A. | 不变 | B. | 不能确定 | C. | 减少 | D. | 增大 |
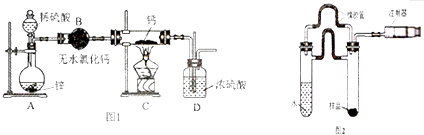
 今有下列气体:H2、Cl2、O2、HCl、NH3、NO(难溶于水).用如图所示装置进行实验,请写下列空白:
今有下列气体:H2、Cl2、O2、HCl、NH3、NO(难溶于水).用如图所示装置进行实验,请写下列空白: