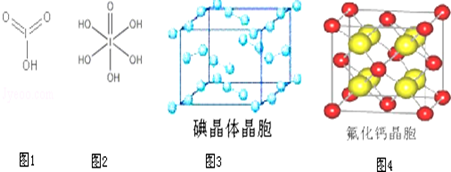
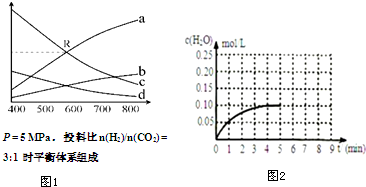
��Ŀ����
20��A��B��C��D 4��Ԫ�أ�AԪ��������������������������ԭ����������ȣ�B��ԭ�Ӱ뾶����������������С�ģ�B������������Ӧˮ����Ļ�ѧʽΪHBO3��CԪ��ԭ�ӵ������������ȴ������2����C����������D�������Ӿ�����ͬ�ĵ����Ų�����Ԫ�ؿ��γɻ�����D2C����1��BԪ�ص����Ƶ���B�����ڱ��е�λ�õڶ����ڣ���VA�壻
��2��A��B�γɵĻ�����ĵ���ʽ
 ��
����3��C��Ԫ�ط���S��C�����������Ļ�ѧʽSO3��
��4��B������������Ӧˮ�����Ũ��Һ�뵥��Cu��Ӧ�Ļ�ѧ��ʽ��ʽCu+4HNO3��Ũ��=Cu��NO3��2+2NO2��+2H2O��
���� A��B��C��D 4��Ԫ�أ�AԪ��������������������������ԭ����������ȣ���AΪHԪ�أ�B��ԭ�Ӱ뾶����������������С�ģ����ڵڶ����ڣ�B������������Ӧˮ����Ļ�ѧʽΪHBO3����������ϼ�Ϊ+5�����ڢ�A�壬��BΪNԪ�أ�CԪ��ԭ�ӵ������������ȴ������2������CӦ���������Ӳ㣬����������Ϊ6����CΪSԪ�أ�C����������D�������Ӿ�����ͬ�ĵ����Ų������Ӻ��������Ϊ18����Ԫ�ؿ��γɻ�����D2C��D�ڵ������ڵڢ�A�壬��DΪK���ݴ˽��
��� �⣺A��B��C��D 4��Ԫ�أ�AԪ��������������������������ԭ����������ȣ���AΪHԪ�أ�B��ԭ�Ӱ뾶����������������С�ģ����ڵڶ����ڣ�B������������Ӧˮ����Ļ�ѧʽΪHBO3����������ϼ�Ϊ+5�����ڢ�A�壬��BΪNԪ�أ�CԪ��ԭ�ӵ������������ȴ������2������CӦ���������Ӳ㣬����������Ϊ6����CΪSԪ�أ�C����������D�������Ӿ�����ͬ�ĵ����Ų������Ӻ��������Ϊ18����Ԫ�ؿ��γɻ�����D2C��D�ڵ������ڵڢ�A�壬��DΪK��
��1��BΪNԪ�أ�λ��Ԫ�����ڱ��еڶ����ڵڢ�A�壬�ʴ�Ϊ�������ڶ����ڵڢ�A�壻
��2��A��B�γɵĻ�����ΪNH3�������ʽΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��3��������������֪��CΪSԪ�أ��������Ϊ+6�������������Ļ�ѧʽΪSO3���ʴ�Ϊ��S��SO3��
��4��B������������Ӧˮ����Ļ�ѧʽΪHNO3��Cu��Ũ���ᷴӦ��������ͭ������������ˮ����Ӧ�ŷ���ʽΪ��Cu+4HNO3��Ũ��=Cu��NO3��2+2NO2��+2H2O���ʴ�Ϊ��Cu+4HNO3��Ũ��=Cu��NO3��2+2NO2��+2H2O��
���� ���⿼��λ�ýṹ���ʵ����ϵӦ�ã��ѶȲ���ע����ȷ�ƶ�Ԫ����Ϊ������Ĺؼ���ע�����յ���ʽ����д��

 ��У����ϵ�д�
��У����ϵ�д���H-�İ뾶��Li+�İ뾶��
��ﮣ�Li���������о���ȼ�գ�������Li2O2������Һ��һ��ǿ��
������At��Ϊ��ɫ���壬HAt���ȶ�
�������⣨H2Se������ɫ���ж�����H2S�ȶ������壮
�������ȣ�SrSO4����������ˮ�İ�ɫ���壮
| A�� | �٢ڢ� | B�� | �٢� | C�� | �ۢܢ� | D�� | �ڢ� |

| A�� | ����ᡢŨ���Ṳ��ʱ���Ѣ� | |
| B�� | ��Ũ��������¼�����170��ʱ���Ѣڢ� | |
| C�� | �ͽ����Ʒ�Ӧʱ���Ѣ� | |
| D�� | ��Cu���º�O2��Ӧʱ���Ѣڢ� |
��R��Yԭ�ӵ���������������Ӳ�����ͬ��
��Q�ǵؿ��к�����ߵ�Ԫ�أ�R��T�ĺ˵����֮�͵���Q�ĺ˵������
��W��Rͬ���壮
| A�� | T��Q��W��Y��ԭ�Ӱ뾶��СΪ��T��Q��Y��W | |
| B�� | Q��W�γɵ����ֳ����������к�����ͬ���������������ӣ�����ͬ�־������� | |
| C�� | Q��Y��ɵij���������һ�ּ��������� | |
| D�� | ��Y��T��ɵ�����YT��ԭ�Ӿ��壬�ڵ��Ӻ��մɹ�ҵ���й㷺Ӧ�ã�����ֱ���ɵ���Y��T�ڵ����ºϳ� |
| A�� | ������������֬���ܷ���ˮ�ⷴӦ���ɴ� | |
| B�� | ��ϩ������ֻ�ܷ����ӳɷ�Ӧ | |
| C�� | ���������������Ƶ�ˮ��Һ�ɷ�Ӧ������ϩ | |
| D�� | ������ʹ����KMnO4��Һ��ɫ |
| A�� | H��D��T��ʾͬһ�ֺ��� | B�� | F-ԭ�ӽṹʾ��ͼ�� | ||
| C�� | �õ���ʽ��ʾHCl�γɹ��� | D�� | NaOH�Ⱥ����ۼ��ֺ����Ӽ� |
| A�� | �ҹ���������Ѿ��ƹ�ʹ�����ȼ���Լ��ٻ�����Ⱦ����ѹ����Ȼ����CNG����Һ��ʯ������LPG����������ȼ�ϵ���Ҫ�ɷ־������� | |
| B�� | ��ˮ�����ķ�����Ҫ�������������������ӽ������� | |
| C�� | ����ʵ��ú���ۺ����õ���Ҫ;����ͨ��ú�ĸ���ú������úҺ������ýྻ��ȼ�ϺͶ��ֻ���ԭ�� | |
| D�� | ��ҵ�����ý��������Բ�ͬ�����ò�ͬ��ұ������ұ�����������ⷨұ�������Ȼ�ԭ��ұ�������ȷֽⷨұ��ͭ |