题目内容
8.短周期原子序数依次增大的主族元素R、T、Q、W、Y具有如下信息:下列说法正确的是( )①R、Y原子的最外层电子数与电子层数相同;
②Q是地壳中含量最高的元素,R与T的核电荷数之和等于Q的核电荷数;
③W与R同主族.
| A. | T、Q、W、Y的原子半径大小为:T<Q<Y<W | |
| B. | Q与W形成的两种常见化合物中含有相同比例的阴、阳离子,属于同种晶体类型 | |
| C. | Q与Y组成的常见物质是一种碱性氧化物 | |
| D. | 由Y和T组成的物质YT是原子晶体,在电子和陶瓷工业上有广泛应用,可以直接由单质Y和T在低温下合成 |
分析 短周期原子序数依次增大的主族元素R、T、Q、W、Y,其中R、Y原子的最外层电子数与电子层数相同,符合条件的元素有H、Be、Al;Q是地壳中含量最高的元素,则Q为O元素;由于R与T的核电荷数之和等于Q的核电荷数,Al原子序数大于O,R为Be时,T的原子序数为4,R、T原子序数相同,故R只能为H元素,则Y为Al;故T的原子序数=8-1=7,即T为N元素;W与R同主族,结合原子序数可知W为Na元素,据此解答.
解答 解:短周期原子序数依次增大的主族元素R、T、Q、W、Y,其中R、Y原子的最外层电子数与电子层数相同,符合条件的元素有H、Be、Al;Q是地壳中含量最高的元素,则Q为O元素;由于R与T的核电荷数之和等于Q的核电荷数,Al原子序数大于O,R为Be时,T的原子序数为4,R、T原子序数相同,故R只能为H元素,则Y为Al;故T的原子序数=8-1=7,即T为N元素;W与R同主族,结合原子序数可知W为Na元素.
A.同主族自上而下原子半径增大,同周期随原子序数增大原子半径减小,故原子半径:O<N<Al<Na,即Q<T<Y<W,故A错误;
B.Q与W形成的两种常见化合物为Na2O、Na2O2,二者含有阴、阳离子之比都是2:1,均属于离子化合物,故B正确;
C.Q与Y组成的常见物质是Al2O3,属于两性氧化物,故C错误;
D.Y和T组成的物质AlN是原子晶体,不能由单质Al和氮气在低温下合成,故D错误,
故选B.
点评 本题考查结构性质位置关系应用,推断元素是解题的关键,对学生的逻辑推理有一定的要求,注意元素周期律的掌握,难度中等.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
18.醋酸钡[(CH3COO)2Ba•H2O]是一种媒染剂,下列是有关0.1mol/L醋酸钡溶液中粒子浓度的比较,其中错误的是( )
| A. | c(H+)=c(OH-)-c(CH3COOH) | B. | c(H+)+2c(Ba2+)=c(CH3COO-)+c(OH-) | ||
| C. | c(Ba2+)>c(CH3COO-)>c(OH-)>c(H+) | D. | 2c(Ba2+)=c(CH3COO-)+c(CH3COOH) |
19.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 1 L 0.1 mol•L-1的氨水中含有的NH3•H2O分子数为0.1 NA | |
| B. | 0.1 mol•L-1 Na2CO3溶液中所含的Na+离子数为0.2 NA | |
| C. | 标准状况下,2.24 L的水含有的分子数为0.1NA | |
| D. | 一定条件下,3.2 g O2和O3混合气体中含有的O原子数目为0.2 NA |
16.几种短周期元素的原子半径及主要化合价见下表
根据表中信息,判断以下说法正确的是( )
| 元素符号 | X | Y | Z | R | T |
| 原子半径(nm) | 0.160 | 0.080 | 0.102 | 0.143 | 0.074 |
| 主要化合价 | +2 | +2 | -2,+4,+6 | +3 | -2 |
| A. | 单质与稀硫酸反应的速率快慢:R>X>Y | |
| B. | 离子半径:T2->X2+ | |
| C. | 元素最高价氧化物的水化物的碱性:X>R>Y | |
| D. | 单质与氢气化合的难易程度:Z>T |
17.甲烷分子中的4个氢原子全部被苯基取代,可得如图所示的分子,对该分子的描述不正确的是( )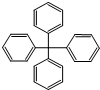

| A. | 分子式为C25H20 | |
| B. | 分子中所有原子有可能处于同一平面 | |
| C. | 该化合物分子中所有原子不可能处于同一平面 | |
| D. | 分子中处于同一平面的原子最多23个 |
18.下列命名正确的是( )
| A. | 3,3-二甲基-4-乙基戊烷 | B. | 3,4,4-三甲基己烷 | ||
| C. | 3,3,4-三甲基戊烷 | D. | 2,3,3-三甲基己烷 |
 (1)BCl3的分子构型sp2.第一电离能介于B、N之间的第二周期元素有3种.写出与BCl3结构相同的一种等电子体NO3-或CO32-(写离子).
(1)BCl3的分子构型sp2.第一电离能介于B、N之间的第二周期元素有3种.写出与BCl3结构相同的一种等电子体NO3-或CO32-(写离子).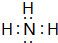 ;
;