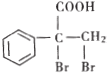
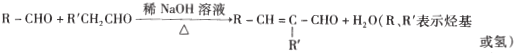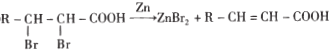题目内容
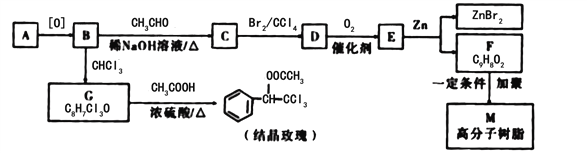
【题目】有关物质的转化关系如下图所示。常温下,B、E呈气态,其中B呈黄绿色。D是最常见的无色液体,E常用作制冷剂,F是一种不溶于水的碱,G是厨房中的常见调味品,H由两种元素组成,其摩尔质量为32 g·mol-1。

(1) E的电子式为____。
(2) H的化学式为____。
(3) 写出反应①的离子方程式:_________________。
(4) 写出反应②的化学方程式:_________________。
【答案】 ![]() N2H4 Cl2+2OH-
N2H4 Cl2+2OH-![]() Cl-+ClO-+H2O Mg3N2+6H2O
Cl-+ClO-+H2O Mg3N2+6H2O![]() 3Mg(OH)2+2NH3↑
3Mg(OH)2+2NH3↑
【解析】B呈黄绿色则为氯气,D是最常见的无色液体,D为水。结合流程可知E常用作制冷剂,由氮化镁与水反应生成,则E为氨气,F是一种不溶于水的碱,F为氢氧化镁;G是厨房中的常见调味品,G为氯化钠;A为氢氧化钠,氢氧化钠与氯气反应生成氯化钠G、次氯酸钠C和水D,次氯化钠与氨气反应生成氯化钠、水和H,H由两种元素组成,其摩尔质量为32 g·mol-1,则H为N2H4;故(1) E为氨气,电子式为![]() ;(2) H的化学式为N2H4;(3) 反应①是氯气与氢氧化钠反应生成氯化钠、次氯酸钠和水,反应的离子方程式为: Cl2+2OH-
;(2) H的化学式为N2H4;(3) 反应①是氯气与氢氧化钠反应生成氯化钠、次氯酸钠和水,反应的离子方程式为: Cl2+2OH-![]() Cl-+ClO-+H2O;(4) 反应②是氮化镁与水反应生成氨气和氢氧化镁,反应的化学方程式为: Mg3N2+6H2O
Cl-+ClO-+H2O;(4) 反应②是氮化镁与水反应生成氨气和氢氧化镁,反应的化学方程式为: Mg3N2+6H2O![]() 3Mg(OH)2+2NH3↑。
3Mg(OH)2+2NH3↑。

 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案 导学教程高中新课标系列答案
导学教程高中新课标系列答案【题目】下列实验能达到预期目的的是
编号 | 实验内容 | 实验目的 |
A | 向含有酚酞的Na2CO3溶液中加入少量BaC12固体,溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
B | 室温下,用pH试纸分别测定浓度为18mol/L和0.1 mol/L H2SO4溶液的pH | 比较不同浓度H2SO4的酸性强弱 |
C | 配制FeCl2溶液时,先将FeCl2溶于适量浓盐酸中,再用蒸馏水稀释到所需浓度,最后在试剂瓶中加入少量铜粉 | 抑制Fe2+水解,并防止Fe2+被氧化 |
D | 向盛有1mL 0.01 mol/L | 证明在相同温度下的 Ksp(AgCl)>Ksp(AgI) |
A. A B. B C. C D. D