题目内容
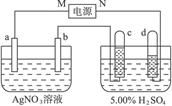
两个串联的电解池A和B,分别盛有AgNO3溶液和NaCl溶液,用惰性电极进行电解,当B池的阴极上收集到2.24 L(标准状况)气体时,在A池的阳极上析出物质多少克?若两种溶液都是2 L,两池溶液的pH各是多少?
1.6 g 1 13
A、B两池发生的反应分别是:
A.4AgNO3+2H2O 4Ag+O2↑+4HNO3
4Ag+O2↑+4HNO3
B.2NaCl+2H2O 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
B池阴极析出H2 2.24 L(标准状况),相当于0.1 mol,电路中应有0.2 mol电子转移。1 mol电子应析出1 mol银,0.5 mol Cl2,0.5 mol H2,0.25 mol O2。
则A池阳极析出O2为0.25 mol/1 mol×0.2 mol×32 g·mol-1=1.6 g,A池中产生0.2 mol H+,溶液的pH=-lg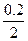 =1。
=1。
B池中生成0.2 mol OH-,溶液的pH=-lg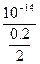 =13。
=13。
A.4AgNO3+2H2O
 4Ag+O2↑+4HNO3
4Ag+O2↑+4HNO3B.2NaCl+2H2O
 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑B池阴极析出H2 2.24 L(标准状况),相当于0.1 mol,电路中应有0.2 mol电子转移。1 mol电子应析出1 mol银,0.5 mol Cl2,0.5 mol H2,0.25 mol O2。
则A池阳极析出O2为0.25 mol/1 mol×0.2 mol×32 g·mol-1=1.6 g,A池中产生0.2 mol H+,溶液的pH=-lg
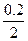 =1。
=1。B池中生成0.2 mol OH-,溶液的pH=-lg
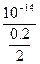 =13。
=13。
练习册系列答案
相关题目
 H<0,
H<0, S>0的化学反应一定能自发进行
S>0的化学反应一定能自发进行