��Ŀ����
����Ŀ���±�ΪԪ�����ڱ���һ���֣������Ԫ���������ڱ��е�λ�ã��ش��������⣺
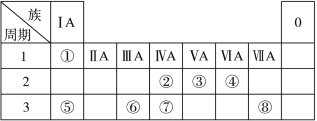
��1���ؿ��к�����ߵĽ���Ԫ�������ڱ��е�λ���� ��
��2�����γɵĵ�����ˮ��Ӧ�����ӷ���ʽΪ ��
��3���ڢ��ķǽ�����ǿ����ͨ���Ƚ�������Ԫ�� (����)
a��ԭ�ӵĵõ��ӵ�����
b�������������
c����̬�⻯����ȶ���
d�����ʵ��۷е�
��4��д��һ�����ܢݢ�Ԫ���γɵļȺ������Ӽ��ֺ��й��ۼ������ʵĵ���ʽ ��
��5��������ҵ����ϳ�����Ԫ���������γɵĻ������Ӳ�ȱȽ��ʯ�����������γɵľ��廹���ܾ��е����ʻ��ص��� (����)
���۵�ܸ�
�����Ե���
�������ڵ�������
�����пռ���״�ṹ
��6���������γɵ�ijҺ̬������Ħ��������������ͬ���ڳ��³�ѹ��0.25 mol��Һ̬��������������������ȫȼ������������̬���ʺ�Һ̬ˮ��ͬʱ�ų�QkJ��������д���÷�Ӧ���Ȼ�ѧ����ʽ____________________________ ______��
���𰸡���1����3���� ��A��
��2��Cl2��H2O![]() HClO��H����Cl��
HClO��H����Cl��
��3��a c(��ѡ��1�֣���ѡ���÷�)
��4��![]() ��
��![]()
��5���� �� ��
��6��N2H4(l)��O2(g) = N2(g)��2H2O(l) H=" ��4Q" kJ��mol��1
�������������������1���ؿ��к�����ߵĽ���Ԫ��Ϊ��Ԫ�أ������ڱ��е�λ���ǵ�3������A�塣
��2����Ϊ��Ԫ�أ�������ˮ��Ӧ��������ʹ����ᣬ���ӷ���ʽΪCl2��H2O![]() HClO��H����Cl����
HClO��H����Cl����
��3����Ϊ̼Ԫ�أ���Ϊ��Ԫ�أ��ǽ�����ǿ����ͨ���Ƚ�ԭ�ӵĵõ��ӵ��������������⻯�ϵ�������̬�⻯����ȶ��ԡ����������ˮ��������Խ��бȽϣ�ѡa��c��
��4����Ϊ��Ԫ�أ���Ϊ��Ԫ�أ���Ϊ��Ԫ�أ������γɵļȺ������Ӽ��ֺ��й��ۼ�������Ϊ�������ƣ�����ʽΪ![]() ��
��![]() ��
��
��5����Ϊ̼Ԫ�أ���Ϊ��Ԫ�أ���������֪�����γɵĻ�����Ϊԭ�Ӿ��壬����Ӳ�ȴ��۵�ߣ������ڵ������ӣ����пռ���״�ṹ�ȣ�ѡ�٢ۢ���
��6����Ϊ��Ԫ�أ���Ϊ��Ԫ�أ������γɵ�ijҺ̬������Ħ��������������ͬ��ΪN2H4���ڳ��³�ѹ��0.25 mol��Һ̬��������������������ȫȼ�����ɵ�����Һ̬ˮ��ͬʱ�ų�QkJ���������÷�Ӧ���Ȼ�ѧ����ʽΪN2H4(l)��O2(g) = N2(g)��2H2O(l) H=" ��4Q" kJ��mol��1��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�