题目内容
【题目】含A元素的一种单质是一种重要的半导体材料,含 A元素的一种化合物C可用于制造高性能的现代通讯材料——光导纤维,C与烧碱反应生成含A元素的化合物D。
(1)A的原子结构示意图为________,A与碳在原子的电子层结构上的相同点是________________________________________________________。
(2)易与C发生化学反应的酸是_________(写名称),反应的化学方程式是_______________________________。
(3)将C与纯碱混合高温熔融时也发生化学反应生成D
①写出该反应的化学方程式:___________________________________________。
②要将纯碱高温熔化,下列坩埚中可选用的是________。
A.普通玻璃坩埚 B.石英玻璃坩埚 C.铁坩埚
(4)100 g C与石灰石的混合物充分反应后,生成的气体在标准状况下的体积为11.2 L,100 g混合物中石灰石的质量分数是________。
【答案】 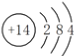 最外层均有4个电子,最内层均有2个电子 氢氟酸 SiO2+4HF===SiF4↑+2H2O SiO2+Na2CO3
最外层均有4个电子,最内层均有2个电子 氢氟酸 SiO2+4HF===SiF4↑+2H2O SiO2+Na2CO3 ![]() Na2SiO3+CO2↑ C 50%
Na2SiO3+CO2↑ C 50%
【解析】试题分析:本题考查无机推断、侧重硅元素的单质及其化合物性质的考查、化学计算。含A元素的一种单质是一种重要的半导体材料,含A元素的一种化合物C可用于制造光导纤维,则A为硅元素,C为SiO2;C(SiO2)与烧碱反应生成Na2SiO3和H2O,含A元素的化合物D为Na2SiO3。
(1)A为Si,Si原子的核电荷数为14,Si原子核外有14个电子,根据原子核外电子排布规律,A的原子结构示意图为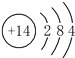 。碳的原子结构示意图为
。碳的原子结构示意图为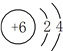 ,硅原子与碳原子的电子层结构上的相同点是:最外层均有4个电子,最内层均有2个电子。
,硅原子与碳原子的电子层结构上的相同点是:最外层均有4个电子,最内层均有2个电子。
(2)C为SiO2,易与SiO2发生化学反应的酸是氢氟酸,SiO2与HF反应生成SiF4和H2O,反应的化学方程式为SiO2+4HF=SiF4↑+2H2O。
(3)①SiO2与纯碱高温熔融时反应生成Na2SiO3和CO2,反应的化学方程式为SiO2+Na2CO3![]() Na2SiO3+CO2↑。
Na2SiO3+CO2↑。
②A,普通玻璃的成分为Na2SiO3、CaSiO3和SiO2,SiO2与纯碱高温下反应生成Na2SiO3和CO2,不能选用普通玻璃坩埚熔化纯碱;B,石英玻璃的成分为SiO2,SiO2与纯碱高温下反应生成Na2SiO3和CO2,不能选用石英玻璃坩埚熔化纯碱;C,铁与Na2CO3高温不反应,可选用铁坩埚熔化纯碱;答案选C。
(4)SiO2与石灰石的混合物充分反应,可能发生的反应有SiO2+CaCO3![]() CaSiO3+CO2↑、CaCO3
CaSiO3+CO2↑、CaCO3![]() CaO+CO2↑,根据C守恒,n(CaCO3)=n(CO2)=
CaO+CO2↑,根据C守恒,n(CaCO3)=n(CO2)=![]() =0.5mol,m(CaCO3)=0.5mol
=0.5mol,m(CaCO3)=0.5mol![]() 100g/mol=50g,100g混合物中石灰石的质量分数为
100g/mol=50g,100g混合物中石灰石的质量分数为![]() 100%=50%。
100%=50%。

【题目】纳米碳酸钙是一种广泛应用于塑料、食品、医药、饲料等行业的重要无机填料。以磷石膏钙渣为原料制取高品质纳米碳酸钙的工艺流程如下:
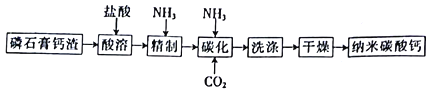
已知某磷石膏钙渣的主要成分及其含量如下表所示。
CaO | P2O5 | SO3 | Fe2O3 | Al2O3 | SiO2 | 烧失量 |
47.70% | 1.60% | 1.77% | 0.041% | 0.0027% | 9.85% | 37.69% |
请回答下列问题:
(1)对磷石膏钙渣进行酸溶的目的是获得机制CaCl2溶液,为了提高溶出率,可以采取的措施有___________(填字母)。
A.粉碎磷石膏钙渣 B.增大盐酸浓度 C.适当降低温度 D.缩短酸溶时间
(2)为了探究酸溶的工艺条件,称取6 份各50g磷石膏钙渣,分别用不同浓度盐酸进行溶解,反应时间为30 min,测得滤液中钙溶出率的结果如图所示,最适宜的盐酸浓度为___________。
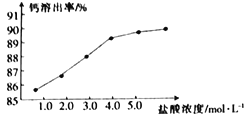
(3)精制是向粗制CaCl2溶液中通入氨气,控制溶液的pH,主要除去___________(填金属阳离子)。
(4)碳化时,先将精制CaCl2溶液稀释至一定体积,控制反应温度以及NH3和CO2 的通入量,此过程中,通入气体有先后顺序,应先通入气体的化学式___________(填化学式);碳化时发生反应的化学方程式为___________________________________________。
(5)把CaCO3浊液滴入1.0mol·L-1 的Na2SO3溶液中,能否产生CaSO3沉淀?___________。若不能,说明原因;若能,请从定量的角度简述判断依据:___________________________________。[已知:Ksp(CaSO3)=1.4×10-7,Ksp(CaCO3)=2.8×10-9
(6)试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级:___________。