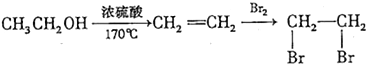题目内容
【题目】在5NH4NO3![]() 2HNO3+4N2↑+9H2O反应中,氧化剂与还原剂物质的量之比是
2HNO3+4N2↑+9H2O反应中,氧化剂与还原剂物质的量之比是
A. 5∶8 B. 5∶4 C. 5∶3 D. 3∶5
【答案】D
【解析】
在氧化还原反应5NH4NO3 ![]() 2HNO3+4N2↑+9H2O中,铵根离子中-3价的N元素的化合价升高,被氧化,铵根离子做还原剂;硝酸根中+5价N元素的化合价降低,被还原,硝酸根做氧化剂,据此判断氧化剂与还原剂的物质的量之比。
2HNO3+4N2↑+9H2O中,铵根离子中-3价的N元素的化合价升高,被氧化,铵根离子做还原剂;硝酸根中+5价N元素的化合价降低,被还原,硝酸根做氧化剂,据此判断氧化剂与还原剂的物质的量之比。
在氧化还原反应5NH4NO3![]() 2HNO3+4N2↑+9H2O中,铵根离子中-3价的N元素的化合价升高,被氧化,铵根离子做还原剂;硝酸根中+5价N元素的化合价降低,被还原,硝酸根做氧化剂,其中有2/5的+5价N没有化合价变化,所以该反应中氧化剂与还原剂的物质的量之比是3:5,故选D。
2HNO3+4N2↑+9H2O中,铵根离子中-3价的N元素的化合价升高,被氧化,铵根离子做还原剂;硝酸根中+5价N元素的化合价降低,被还原,硝酸根做氧化剂,其中有2/5的+5价N没有化合价变化,所以该反应中氧化剂与还原剂的物质的量之比是3:5,故选D。

练习册系列答案
相关题目
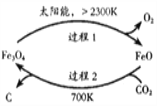
【题目】一定条件下,下列各组物质能一步实现图中所示转化关系的是
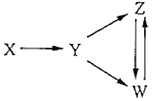
选项 | X | Y | Z | W |
A | Al | Al2O3 | NaAlO2 | Al(OH)3 |
B | Fe3O4 | Fe | FeCl2 | FeCl3 |
C | H2SO4 | SO2 | S | SO3 |
D | CH3CH2Br | CH2=CH2 | C2H5OH | CH2BrCH2Br |
A. A B. B C. C D. D