题目内容
【题目】Fe2O3+2Al![]() Al2O3+2Fe所属基本反应类型是________。在该反应中________元素的化合价升高,该元素的原子________电子,被________;该反应中,________是氧化剂,________是氧化产物;氧化剂与还原剂的物质的量之比为___________;用双线桥标出该反应中电子转移的方向和数目_______________。
Al2O3+2Fe所属基本反应类型是________。在该反应中________元素的化合价升高,该元素的原子________电子,被________;该反应中,________是氧化剂,________是氧化产物;氧化剂与还原剂的物质的量之比为___________;用双线桥标出该反应中电子转移的方向和数目_______________。
【答案】 置换反应 铝 失 氧化 Fe2O3 Al2O3 1:2 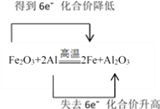
【解析】此反应为一种单质与一种化合物反应生成另一种单质和另一种化合物的反应,从反应类型上看该反应是置换反应;在该反应中,铝元素的化合价由0价升高到+3价,失去电子,被氧化,发生氧化反应,铝为还原剂,对应的产物氧化铝为氧化产物;氧化铁中的铁元素化合价由+3价降低到0价,得到电子,被还原,发生还原反应,氧化铁为氧化剂,对应的产物单质铁为还原产物;根据得失电子守恒,用双线桥法表示的式子为: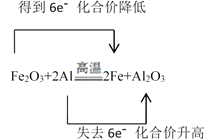 ,根据上述分析可知,本题的答案为:置换反应;铝;失;氧化;Fe2O3;Al2O3;1:2;
,根据上述分析可知,本题的答案为:置换反应;铝;失;氧化;Fe2O3;Al2O3;1:2; 。
。

练习册系列答案
相关题目