题目内容
【题目】下列装置或操作能达到目的的是
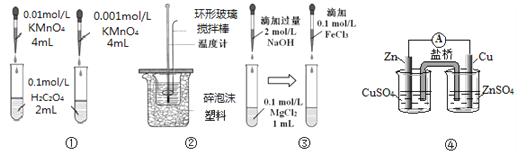
A. 装置①依据褪色快慢探究浓度对反应速率的影响 B. 装置②可用于测定中和热
C. 装置③探究Mg(OH)2能否转化成Fe(OH)3 D. 装置④构成锌—铜原电池
【答案】B
【解析】A.高锰酸钾溶液的浓度、体积不同,无法探究浓度对反应速率的影响;B.满足中和热测定的要求;C.由于滴加了过量的氢氧化钠溶液,氯化铁可以与氢氧化钠反应生成Fe(OH)3;D.锌电极插入硫酸锌溶液,铜电极插入硫酸铜溶液,才能构成原电池。
不同浓度、不同体积的高锰酸钾溶液与同浓度、同体积的草酸反应,不能依据褪色快慢探究浓度对反应速率的影响,A错误;装置②可用于测定中和热,B正确;由于滴加了过量的氢氧化钠溶液,氯化铁可以与氢氧化钠反应生成Fe(OH)3 ,不能达到实验目的,C错误;锌棒插入硫酸锌溶液,铜插入硫酸铜溶液,构成原电池,装置④不能构成锌—铜原电池,D错误;正确选项B。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
【题目】N2O5是一种新型硝化剂,在一定温度下可发生如下反应:2N2O5(g)![]() 4NO2(g)+O2(g) △H>0。T1温度时,向密闭容器中通入N2O5气体,部分实验数据见下表:
4NO2(g)+O2(g) △H>0。T1温度时,向密闭容器中通入N2O5气体,部分实验数据见下表:
时间/s | 0 | 500 | 1000 | 1500 |
c(N2O5)/(mol·L—1) | 5.00 | 3.52 | 2.50 | 2.50 |
下列说法正确的是
A. 500s内O2的平均生成速率为7.4×l0—4mol·L—1·s—1
B. T1温度下该反应达到平衡时,平衡混合物中NO2的体积分数为50%
C. 达到平衡后,其他条件不变,将容器体积压缩到原来的1/2,则c(N2O5)>5.00mol·L—1
D. T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若K1<K2,则T1>T2