题目内容
【题目】I.(1)写出H2CO3的电离方程式:__________________________________________。
(2)现有①CH3COOH、②HCl两种溶液,选择填空:
A.①>② B.①<② C.①﹦②
①当它们物质的量浓度相等时,中和等体积、等物质的量浓度的烧碱溶液需两种酸溶液的体积关系为____________。
②当它们氢离子浓度相同、体积相同时,分别加入足量锌,相同状况下产生气体体积关系为____________。
II.煤化工产业中常用合成气(主要成分是氢气和一氧化碳气体)合成氨和甲醇。请回答:
(1)工业合成氨的化学方程式为N2+3H2![]() 2NH3 ,在某压强恒定的密闭容器中加入2 mol N2和4 mol H2,达到平衡时,N2的转化率为50%,体积变为10 L。则该条件下的平衡常数为________。
2NH3 ,在某压强恒定的密闭容器中加入2 mol N2和4 mol H2,达到平衡时,N2的转化率为50%,体积变为10 L。则该条件下的平衡常数为________。
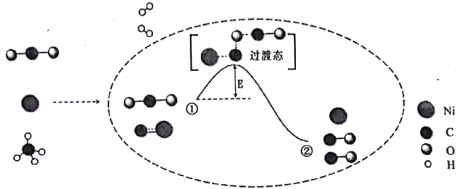
(2)合成甲醇的主要反应是2H2(g)+CO(g)![]() CH3OH(g) ΔH=-90.8 kJ·mol-1,t ℃下此反应的平衡常数为160。此温度下,在密闭容器中开始只加入CO、H2,反应10 min后测得各组分的浓度如:
CH3OH(g) ΔH=-90.8 kJ·mol-1,t ℃下此反应的平衡常数为160。此温度下,在密闭容器中开始只加入CO、H2,反应10 min后测得各组分的浓度如:
物质 | H2 | CO | CH3OH |
浓度(mol·L-1) | 0.2 | 0.1 | 0.4 |
①该时间段内反应速率v(H2)=________。
②比较此时正、逆反应速率的大小:v正________v逆(填“>”、“<”或“=”)。
③反应达到平衡后,保持其它条件不变,若只把容器的体积缩小一半,平衡______(填“逆向”、“正向”或“不”)移动,平衡常数K_________(填“增大”、“减小”或“不变”)。
【答案】H2CO3![]() H++HCO3- 、HCO3-
H++HCO3- 、HCO3-![]() H++CO32- C A 400 0.08 molL-1min-1 > 正向 不变
H++CO32- C A 400 0.08 molL-1min-1 > 正向 不变
【解析】
I.(1)H2CO3是二元弱酸,属于弱电解质,电离时部分电离,则其电离方程式为:H2CO3![]() H++HCO3-、HCO3-
H++HCO3-、HCO3-![]() H++CO32-
H++CO32-
(2)①CH3COOH、HCl二者中和等体积、等物质的量浓度的烧碱溶液所消耗的物质的量相同,当二者的物质的量浓度相同时,所消耗的体积也相同,答案选C;
②当它们氢离子浓度相同、体积相同时,因为CH3COOH为弱电解质,在水溶液中部分电离,HCl是强电解质,在水溶液中完全电离,故CH3COOH的物质的量浓度应大于HCl的物质的量浓度,体积相同时,则![]() ,分别加入足量锌,CH3COOH反应所生成氢气体积多于HCl反应产生的氢气体积,答案选A。
,分别加入足量锌,CH3COOH反应所生成氢气体积多于HCl反应产生的氢气体积,答案选A。
II.(1)设H2的转化量为x,NH3的转化量为y
由题可知,N2转化量=![]()
N2 + 3H2 ![]() 2NH3
2NH3
起始量/mol 2 4 0
转化量/mol 1 x y
平衡量/mol 1 4-x y
H2的转化量![]() ,H2的平衡量为
,H2的平衡量为![]()
NH3的转化量/平衡量![]()
则![]() ,
,![]() ,
,![]()
其平衡常数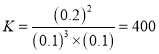 ,答案为:400;
,答案为:400;
(2)①由题可知,CH3OH起始浓度为0,10min后浓度为0.4 mol·L-1,则![]() 根据同一反应中各物质的化学反应速率之比等于相应各物质的化学计量数之比,可知
根据同一反应中各物质的化学反应速率之比等于相应各物质的化学计量数之比,可知![]() ;
;
②10min后浓度商![]() ,
,![]() ,则反应正反应方向移动,此时
,则反应正反应方向移动,此时![]() ,故答案为:>;
,故答案为:>;
③平衡后,其他条件不变,把容器的体积缩小一半,相当于增大压强,可逆反应向气体体积减小的方向移动,即反应向正反应方向移动;平衡常数只与温度有关,温度不变,平衡常数不变。故答案为:正向;不变。

 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案【题目】高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如下图所示。回答下列问题:
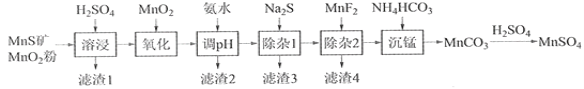
相关金属离子[c0(Mn+)=0.1 mol·L1]形成氢氧化物沉淀的pH范围如下:
金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ | Zn2+ | Ni2+ |
开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
(1)“滤渣1”含有S和__________________________;写出“溶浸”中二氧化锰与硫化锰反应的化学方程式_______________________________________。
(2)“氧化”中添加适量的MnO2的作用是将________________________,检验生成离子试剂___________。
(3)“调pH”除铁和铝,溶液的pH范围应调节为_______~6之间,除铝的离子反应方程式是__________。
(4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是______________。
(5)氧化中除了添加适量MnO2还可以用H2O2来氧化,写出该离子反应_______________。
(6)写出“沉锰”的离子方程式_______________________________________。
(7)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为LiNixCoyMnzO2,其中Ni、Co、Mn的化合价分别为+2、+3、+4。当x=y=![]() 时,z=___________。
时,z=___________。
(8)写出Fe2+和HNO3的离子反应__________。