题目内容
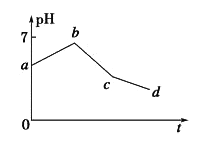
【题目】用石墨作电极电解KCl和CuSO4(等体积混合)混合溶液,电解过程中溶液pH随时间t的变化如图所示,下列说法正确的是
A. ab段H+被还原,溶液的pH 增大
B. cd 段相当于电解水
C. c点时加人适量CuCl2固体,电解液可恢复原来浓度
D. 原溶液中KCl和CuSO4的物质的量浓度之比为2:1
【答案】B
【解析】用惰性电极电解等体积的KCl和CuSO4混合溶液,阴极离子放电顺序是Cu2+>H+,阳极上离子放电顺序是Cl->OH-,电解过程中分三段:第一阶段:阳极上电极反应式为2Cl--2e-=Cl2↑、阴极电极反应式为Cu2++2e-=Cu,铜离子浓度减小,水解得到氢离子浓度减小,溶液pH上升;第二阶段:阳极上电极反应式为4OH--4e-=2H2O+O2↑,阴极反应先发生Cu2++2e-=Cu,反应中生成硫酸,溶液pH降低;第三阶段:阳极电极反应式为4OH--4e-=2H2O+O2↑、阴极电极反应式为2H++2e-=H2↑,实质是电解水,溶液中硫酸浓度增大,pH继续降低。
A.ab段由于铜离子浓度减小,水解得到氢离子浓度减小,溶液pH上升,铜离子为被还原,A错误;B.由上述分析可知,cd 段相当于电解水,B正确;C.电解至c点时,溶液中溶质为硫酸、硫酸钾,往电解液中加入适量CuCl2固体,不能使电解液恢复至原来的浓度,C错误;D.图象中具体数量关系未知,不能计算原混合溶液中KCl和CuSO4的浓度之比,D错误,答案选B。

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案
相关题目