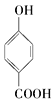
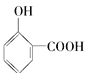
题目内容
【题目】为测定某有机化合物A的结构,进行如下实验:
(1)将有机物A置于O2流中充分燃烧,实验测得:生成5.4gH2O和8.8gCO2,消耗O26.72L(标准状况下),则该物质中各元素的原子个数比为________________。
(2)用质谱仪测定该有机化合物的相对分子质量,该物质的分子式是_____________。
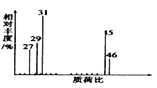
(3)核磁共振氢谱能对有机物分子中不同化学环境的氢原子给出不同的峰值(信号),根据峰值(信号)可以确定分子中氢原子的种类和数目。经测定,有机物A的核磁共振氢谱示意图如下右图,则A的结构简式为________________。
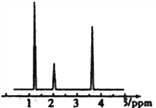
(4)A在一定条件下脱水可生成B,B可合成包装塑料C,请写出B转化为C的化学反应方程式:____________。
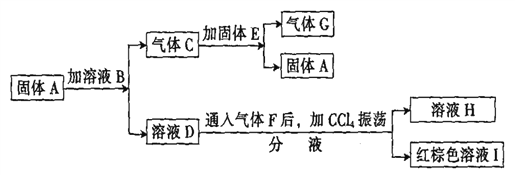
(5)下列物质都是有机化合物,其中C8H10为一取代芳烃,且F不含甲基,转化关系如下:
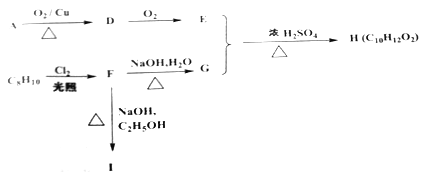
①请写出由F生成I的化学方程式:_____________。
②与H的官能团相同,且苯环上只有一取代的同分异构体共有_________种(不包括H),写出其中任意一个能发生银镜反应的有机物的结构简式:____________。
【答案】 N(C):N(H):N(O)=2:6:1 C2H6O CH3CH2OH ![]()
![]() 14
14 
【解析】试题分析:(1)根据元素守恒计算各元素的原子个数比为;(2)用质谱仪测定该有机化合物的相对分子质量为46;(3)根据核磁共振氢谱,分子中有3种不同环境的氢原子,个数比为3:2:1;(4) A在一定条件下脱水可生成B,B中含有不饱和键,发生加成反应,合成包装塑料;(5) C8H10为一取代芳烃,C8H10是乙苯,且F不含甲基,F是![]() ,F消去生成I,I是苯乙烯;根据流程,
,F消去生成I,I是苯乙烯;根据流程,![]() 发生水解反应生成G,G是苯
发生水解反应生成G,G是苯![]() ;
;
;A是乙醇、D是乙醛、E是乙酸,![]() 与乙酸酯化生成H,H是
与乙酸酯化生成H,H是![]() ;
;
解析:(1) 5.4gH2O的物质的量是0.3mol、8.8gCO2的物质的量是0.2mol,则C、H、O的物质的量分别是0.2mol、0.6mol、0.7mol,消耗O2 6.72L(标准状况下),氧气物质的量是0.3mol,则该物质中C、H、O的物质的量分别是0.2mol、0.6mol、0.1mol,各元素的原子个数比为2:6:1。
(2)用质谱仪测定该有机化合物的相对分子质量为46,该物质的分子式是C2H6O;
(3)根据核磁共振氢谱,分子中有3种不同环境的氢原子,个数比为3:2:1,则该物质的结构简式为CH3CH2OH;(4) CH3CH2OH脱水可生成乙烯,乙烯可合成聚乙烯C,化学反应方程式为![]() ;(5)根据以上分析,①请写出由
;(5)根据以上分析,①请写出由![]() 发生消去反应生成苯乙烯的化学方程式
发生消去反应生成苯乙烯的化学方程式![]() 。
。
②含有酯基、苯环上只有一取代![]() 的同分异构体共有
的同分异构体共有
共14种;能发生银镜反应的有机物的结构为甲酸酯,结构简式为

 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案