题目内容
【题目】0.1mol某元素的单质直接与足量氯气反应,质量增加7.1g,这种元素可能是( )
A. NaB. CuC. FeD. Al
【答案】B
【解析】
固体质量增加7.1g,则参加反应的氯气质量为7.1g,其物质的量为![]() =0.1mol,这说明单质和氯气按物质的量之比1:1进行反应。则
=0.1mol,这说明单质和氯气按物质的量之比1:1进行反应。则
A.钠与氯气反应为2Na+Cl2![]() 2NaCl,钠与氯气按物质的量比2∶1反应,故A不选;
2NaCl,钠与氯气按物质的量比2∶1反应,故A不选;
B.Cu与氯气反应为Cu+Cl2![]() CuCl2,Cu与氯气按物质的量比1∶1反应,故B选;
CuCl2,Cu与氯气按物质的量比1∶1反应,故B选;
C.铁与氯气反应为2Fe+3Cl2![]() 2FeCl3,铁与氯气按物质的量比2∶3反应,故C不选;
2FeCl3,铁与氯气按物质的量比2∶3反应,故C不选;
D.铝与氯气反应为2Al+3Cl2![]() 2AlCl3,铝与氯气按物质的量比2∶3反应,故D不选;
2AlCl3,铝与氯气按物质的量比2∶3反应,故D不选;
故选B。

【题目】硫酸锌可用于制造锌钡白、印染媒染剂等。用锌白矿(主要成分为ZnO,还含有Fe2O3、CuO、SiO2等杂成) 制备ZnSO4 ·7H2O的流程如下。
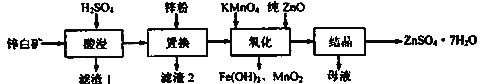
相关金属离了生成氢氧化物沉淀的pH (开始沉淀的pH按金属离子浓度为1.0mol·L-1计算)如下表:
金属离子 | 开始沉淀的pH | 沉淀完全的pH |
Fe3+ | 1.1 | 3.2 |
Fe2+ | 5.8 | 8.8 |
Zn2+ | 6.4 | 8.0 |
(1)“滤渣1”的主要成分为_________(填化学式)。“酸浸”过程中,提高锌元素浸出率的措施有:适当提高酸的浓度、______________(填一种)。
(2)“置换”过程中,加入适量的锌粉,除与溶液中的Fe3+,H+反应外,另一主要反应的化学方程式为__________________________。
(3)“氧化”一步中,发生氧化还原反应的离子方程式为_______________________。溶液pH控制在[3.2,6.4)之间的目的是_______________________________。
(4)“母液”中含有的盐类物质有_________ (填化学式)。
(5)ZnSO4 ·7H2O可用于配制铁件上镀锌电镀池的电解液,下列说法不正确的是_______
A.配制一定物质的量浓度ZnSO4溶液时必需的玻璃仪器为容量瓶、烧杯、玻璃棒
B.电镀池的阳极为铁件
C.阴极质量增加65g时,理论上导线中通过2mol电子
D.电镀过程中电解质溶液的浓度不变








