题目内容
用NA表示阿伏加德罗常数,下列说法正确的是
| A.常温常压下,4.4g CO2和4.4g N2O的原子总数都是0.3NA |
| B.次氯酸光照分解产生22.4mL气体(标准状况下),转移电子数为0.002NA |
| C.常温下,4.6g乙醇含有C—H键总数为0.6 NA |
| D.0.2 mol·L-1 FeCl3溶液中含有Cl-总数为0.6NA |
A
解析试题分析:由于二氧化碳和一氧化二氮的相对分子质量都是44,n=m/M,则n(CO2)=0.1mol,n(N2O)=0.1mol,由于1个二氧化碳分子含有3个原子、1个一氧化二氮分子含有3个原子,则0.1mol二氧化碳分子含有0.3mol原子、0.1mol一氧化二氮分子含有0.3mol原子,故A选项正确;根据次氯酸的性质及化合价升降总数等于转移电子数可得:2HClO 2HCl+O2↑~4e—,由于n=V/22.4L?mol—1,则n(O2)=0.001mol,转移电子与氧气的系数之比等于物质的量之比,则每产生0.001mol氧气,次氯酸分解反应转移0.004mol电子,故B选项错误;由于乙醇的相对分子质量为46,n=m/M,则n(C2H5OH)=0.1mol,由于1个乙醇分子中含有5个C—H键、1个C—C键、1个O—H键,则0.1mol乙醇含有0.5molC—H键,故C选项错误;由于溶液的体积未知,不能根据c?V求出氯化铁的物质的量,也不能求氯离子的物质的量,故D选项错误。
2HCl+O2↑~4e—,由于n=V/22.4L?mol—1,则n(O2)=0.001mol,转移电子与氧气的系数之比等于物质的量之比,则每产生0.001mol氧气,次氯酸分解反应转移0.004mol电子,故B选项错误;由于乙醇的相对分子质量为46,n=m/M,则n(C2H5OH)=0.1mol,由于1个乙醇分子中含有5个C—H键、1个C—C键、1个O—H键,则0.1mol乙醇含有0.5molC—H键,故C选项错误;由于溶液的体积未知,不能根据c?V求出氯化铁的物质的量,也不能求氯离子的物质的量,故D选项错误。
考点:考查阿伏加德罗常数,涉及物质的量、质量、摩尔质量、体积、气体摩尔体积、物质的量浓度之间的计算,以及物质的组成和结构、氧化还原反应中转移电子数、物质的量在化学(或电离)方程式(或关系式)中的应用、强电解质等。

练习册系列答案
相关题目
NA代表阿伏加德罗常数,下列说法正确的是:( )
| A.分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28 g |
B.已知2CO(g)+O2(g)  2CO2(g);△H=-akJ﹒mol-1将2NA个CO与NA个O2混合充分反应放出akJ的热量。 2CO2(g);△H=-akJ﹒mol-1将2NA个CO与NA个O2混合充分反应放出akJ的热量。 |
| C.用石灰乳完全吸收l mol Cl2时,转移电子的数目是NA |
| D.常温下,0.1mol/LNa2CO3溶液中,含有阴离子的总数大于0.1NA |
NA代表阿伏加德罗常数。下列叙述正确的是
| A.标准状况下,22.4L己烷中C-C共价键数目为5NA |
| B.0.1mol·L¯1AlCl3溶液中含有氯离子数为0.3NA |
| C.1molFe在1molCl2中充分燃烧,转移电子数为3NA |
| D.20g重水(2 1H2O)所含的电子数为10NA |
下列有关说法正确的是
| A.7.45gNaClO中含有6.02×1022个NaClO分子 |
| B.1.00 molNaClO中所有ClO-的电子总数为26×6.02×1023 |
| C.1 L2 mol/L明矾经水解可得到氢氧化铝胶体粒子数目为2×6.02×1023 |
| D.将2.00 mol明矾完全溶于1.00 L 水中,得到溶液的物质的量浓度为2 mol/L |
用NA表示阿伏加德罗常数,下列叙述正确的是(相对原子质量:N—14 H—1)
| A.1L0.1mol?L―lNaHCO3溶液中含有0.1NA个HCO3― |
| B.17g氨气中含有的氢原子数为3NA |
| C.标准状况下,2.24LC2H4中含共价键数为0.4NA |
| D.常温常压下,2.24L甲烷中含有甲烷分子数为0.1NA |
NA为阿伏加德罗常数的数值,下列叙述正确的是
| A.22.4L NH3中含氮原子数为NA |
| B.1 mol Na2O2与水完全反应时转移的电子数为NA |
| C.1 L 0.1mol·L-1碳酸钠溶液的阴离子总数等于0.1 NA |
| D.1 mol O2和2 mol SO2在密闭容器中充分反应后的分子数等于2NA |
用NA表示阿伏加德罗常数的值,下列叙述中正确的是
| A.通常情况下,7.6g CS2含有非极性键数目为0.4NA |
| B.22.4L CO气体与1mol N2所含的电子数相等 |
| C.将7.8gNa2O2放入足量的水中,反应时转移0.1NA电子 |
| D.25℃时,1L pH=13的Ba(OH)2溶液中含OH—数目为0.2NA |
下列电子式书写正确的是
A.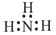 | B.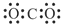 | C.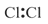 | D.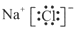 |