��Ŀ����
����Ŀ��ij�¶�ʱ����һ��2 L���ܱ������У�X��Y��Z�������ʵ����ʵ�����ʱ��ı仯������ͼ��ʾ������ͼ�����ݣ�����д���пհף�
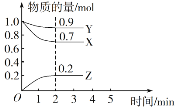
��1���÷�Ӧ�Ļ�ѧ����ʽΪ_______________��
��2����Ӧ��ʼ��2 min��������Z��ʾ��ƽ����Ӧ����Ϊ________��
��3�������ж�������Ӧ�Ѿ��ﵽƽ�����________��
A��v(A)��v (B)��v (C)���ڻ�ѧ������֮��
B���ܱ���������ѹǿ���� C���ܱ������л��������ܶȲ���
D����������ƽ����Է����������ٸı� E��n(A)��n(B)��n(C)���ڻ�ѧ������֮��
���𰸡�3X+Y ![]() 2Z 0.05mol/(l.min) BD
2Z 0.05mol/(l.min) BD
��������
��1����Ӧ������ʵ������٣�����������ʵ��������࣬�������ʵ����ı仯�жϼ�����֮��Ĺ�ϵ��
��2������![]() ����������Z��ʾ��ƽ����Ӧ���ʣ�
����������Z��ʾ��ƽ����Ӧ���ʣ�
��3������ƽ���־�ж��Ƿ�ﵽƽ��״̬��
��1����ͼ���֪��Z�����ʵ��������࣬X��Y�����ʵ������٣���X��YΪ��Ӧ�ZΪ���������ȵ�ʱ����X��Y��Z�����ʵı仯֮��Ϊ0.3:0.1:0.2=3:1:2�����Է�Ӧ����ʽӦΪ��3X+Y![]() 2Z��
2Z��
��2��![]() 0.05mol/(L��min)��
0.05mol/(L��min)��
��3��A������ʱ�̣�����Ӧ�����ʱȶ�����ϵ���ȣ�����v(A)��v(B)��v(C)���ڻ�ѧ������֮�Ȳ�һ��ƽ�⣬�ʲ�ѡA��
B��3X+Y![]() 2Z��Ӧǰ���������ʵ����DZ������ں�����������ѹǿ�DZ�������ѹǿ����һ��ƽ�⣬��ѡB��
2Z��Ӧǰ���������ʵ����DZ������ں�����������ѹǿ�DZ�������ѹǿ����һ��ƽ�⣬��ѡB��
C��![]() ��3X+Y
��3X+Y![]() 2Z��Ӧǰ�������������Ǻ������ں��������з�Ӧ���ܶ��Ǻ��������������ܶȲ��䲻һ��ƽ�⣬�ʲ�ѡC��
2Z��Ӧǰ�������������Ǻ������ں��������з�Ӧ���ܶ��Ǻ��������������ܶȲ��䲻һ��ƽ�⣬�ʲ�ѡC��
D��3X+Y![]() 2Z��Ӧǰ���������ʵ����DZ�����
2Z��Ӧǰ���������ʵ����DZ�����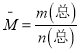 ����������ƽ����Է��������DZ�������������ƽ����Է����������ٸı�һ���ﵽƽ��״̬����ѡD��
����������ƽ����Է��������DZ�������������ƽ����Է����������ٸı�һ���ﵽƽ��״̬����ѡD��
E��n(A)��n(B)��n(C)���ڻ�ѧ������֮��ʱ��Ũ�Ȳ�һ�����ٱ仯�����Բ�һ��ƽ�⣬�ʲ�ѡE��

 ������ϵ�д�
������ϵ�д� �±�Сѧ��Ԫ�Բ���ϵ�д�
�±�Сѧ��Ԫ�Բ���ϵ�д�����Ŀ������ͼװ���о��绯ѧԭ�������з����д������
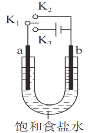
ѡ�� | ���� | �缫���� | ���� | |
a | b | |||
A | K1K2 | ʯī | �� | ģ������������ʴ |
B | K1K2 | п | �� | ģ������������������������������� |
C | K1K3 | ʯī | �� | ģ���ⱥ��ʳ��ˮ |
D | K1K3 | �� | ʯī | ģ�������������ӵ��������������� |
A. A B. B C. C D. D

