题目内容
18.制取CH3CH2Cl,采用的最佳方法是( )| A. | 乙烷和氯气取代反应 | B. | 乙烯和氯气加成反应 | ||
| C. | 乙烯和HCl加成反应 | D. | 乙烷和HCl作用 |
分析 制备一氯乙烷可用乙烯加成法、乙烷取代法等方法,最好的方法是乙烯加成的方法,没有副产品,得到的产物较为纯净.
解答 解:A.乙烷和氯气取代反应可生成一氯乙烷、二氯乙烷等多种取代物,产品不纯,且难以分离,故A错误;
B.乙烯和氯气加成反应生成二氯乙烷,不是一氯乙烷,故B错误;
C.乙烯和HCl加成反应只生成一氯乙烷,得到的产物较为纯净,故C正确;
D.乙烷和盐酸不反应,故D错误.故选C.
点评 本题考查一氯乙烷的制备方案的设计,题目难度不大,本题注意最佳方案的评价以及有机物的性质.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
14.下列反应中,氧化反应与还原反应在同一元素中进行的是( )
| A. | 2FeC12+C12=2FeC13 | B. | Fe+CuSO4=Cu+FeSO4 | ||
| C. | C12+2NaOH=NaC1+NaC1O+H2O | D. | 2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑ |
9.下列实验装置能达到实验目的是( )
| A. | 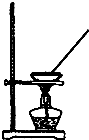 如图所示装置获得碳酸氢钠固体 | B. | 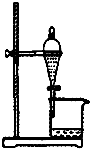 如图所示装置分离乙酸和乙酸乙酯 | ||
| C. | 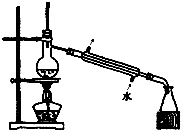 如图所示装置制取少量蒸馏水 | D. | 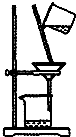 如图所示装置提纯氢氧化铁胶体 |
6.下列关于平衡常数的说法正确的是( )
| A. | 改变外界条件使化学平衡状态改变时,平衡常数也一定改变 | |
| B. | 改变条件,反应物的转化率增大,平衡常数一定增大 | |
| C. | 若一个可逆反应的平衡常数很大,则反应会在较短的时间内完成 | |
| D. | 已知2NO2?N2O4正反应的平衡常数为K1,逆反应的平衡常数为K2,则K1=$\frac{1}{{K}_{2}}$ |
13.下列说法正确的是( )
| A. | 常温时,某溶液中由水电离出来的c(H+)和c(OH-)的乘积为1×10-24,该溶液中一定可以大量存在:K+、Na+、AlO2-、SO42- | |
| B. | 向1 mo1•L-l CH3COOH溶液中加入少量CH3COONa固体,由于CH3COONa水解显碱性,所以溶液的pH升高 | |
| C. | 25℃时,将a mo1•L-l氨水与0.01 moI•L-1盐酸等体积混合,反应完全时溶液中c(NH4+)=c(C1-),用含a的代数式表示反应完全时NH3•H2O的电离常数Kb=$\frac{1{0}^{-9}}{a-0.01}$ | |
| D. | 已知298K时,MgCO3的Ksp=6.82×10-6,溶液中c(Mg2+)=0.0001 mol•L-1,c(CO32-)=0.0001 mol•L-1,此时Mg2+和CO32-不能共存 |
3.下列方法可用于分离、提纯固态有机物的是( )
| A. | 蒸馏 | B. | 分馏 | C. | 重结晶 | D. | 萃取 |
10.下列有机化合物的分类不正确的是( )
| A. |  苯的同系物 | B. | 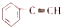 芳香烃 | C. |  卤代烃 | D. | 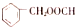 酯 |
7.下列反应中,能够说明乙烯分子具有不饱和键的是( )
| A. | 加成反应 | B. | 取代反应 | C. | 燃烧 | D. | 氧化反应 |
8.下列说法不正确的是( )
| A. | 各种物质都储存有化学能 | |
| B. | 化学反应一定伴随着能量的变化 | |
| C. | 断开反应物中的化学键要释放出能量 | |
| D. | 化学反应中的能量变化,通常主要表现为热量变化 |