题目内容
(6分)将6molA气体和2molB气体在2L密闭容器中混合并在一定条件下发生反应:3A(g)+B(g) xC(g)+2D(g)。若经5min后反应达到平衡状态,容器内的压强变小,并知D的平均反应速率为0.2mol/(L?min),请填写下列空白:
xC(g)+2D(g)。若经5min后反应达到平衡状态,容器内的压强变小,并知D的平均反应速率为0.2mol/(L?min),请填写下列空白:
①x的数值为 ; ②A的平均反应速率为 ; ③5min时B的转化率为 。
 xC(g)+2D(g)。若经5min后反应达到平衡状态,容器内的压强变小,并知D的平均反应速率为0.2mol/(L?min),请填写下列空白:
xC(g)+2D(g)。若经5min后反应达到平衡状态,容器内的压强变小,并知D的平均反应速率为0.2mol/(L?min),请填写下列空白:①x的数值为 ; ②A的平均反应速率为 ; ③5min时B的转化率为 。
① 1 ②0.3mol?L-1?min -1 ③50%
试题分析:①由于反应达到平衡时容器内的压强变小,则该反应的正反应是个气体体积减小的反应,所以3+1>x+2.方程式的系数都是正整数。所以x=1。②V(D)= 0.2mol/(L?min),由于V(A):V(D)=3:2,所以V(A)= (0.2mol/(L?min)×3)÷2=0.3mol/(L?min)。③5min时V(D)= 0.2mol/(L?min),由于V(B):V(D)=1:2;所以V(B)= 0.1mol/(L?min);Δc(B)= V(B)·Δt=0.1mol/(L?min)×5min=0.5mol/L因此B的转化率为{0.5mol/L÷(2mol÷2L)}×100% =50% .

练习册系列答案
相关题目
 FeO(s)+CO(g) ΔH1=akJ·mol一
FeO(s)+CO(g) ΔH1=akJ·mol一
 2CO(g)+2H2(g) △H= kJ·mol-1
2CO(g)+2H2(g) △H= kJ·mol-1

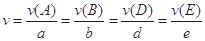 。式中
。式中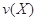 指物质
指物质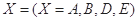 的反应速率,
的反应速率,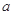 、
、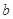 、
、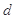 、
、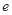 是化学计量数。298k时,测得溶液中的反应H2O2+2HI=2H2O+I2在不同浓度时化学反应速率v见下表:
是化学计量数。298k时,测得溶液中的反应H2O2+2HI=2H2O+I2在不同浓度时化学反应速率v见下表: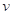 (H2O2)相等
(H2O2)相等 30S内,NO增加了0.3mol,则在30S内,该反应的平均反应速率正确的是
30S内,NO增加了0.3mol,则在30S内,该反应的平均反应速率正确的是  H=-1266.8kJ·mol-1
H=-1266.8kJ·mol-1
 Si3N4 + 6CO,该反应过程中的能量变化如图⑵所示;回答下列问题:
Si3N4 + 6CO,该反应过程中的能量变化如图⑵所示;回答下列问题: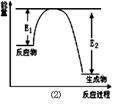

 (正)
(正) 
