题目内容
CuSO4·5H2O是铜的重要化合物,有着广泛的应用。以下是CuSO4·5H2O的实验室制备流程图。
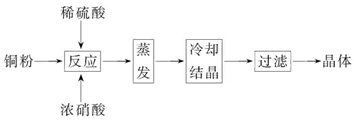
根据题意完成下列填空:
(1)向含铜粉的稀硫酸中滴加浓硝酸,在铜粉溶解时可以观察到的实验现象:_____________、_____________。
(2)如果铜粉、硫酸及硝酸都比较纯净,则制得的CuSO4·5H2O中可能存在的杂质是_____________,除去这种杂质的实验操作称为_____________。
(3)已知:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4。称取0.100 0 g提纯后的CuSO4·5H2O试样于锥形瓶中,加入0.100 0 mol/L氢氧化钠溶液28.00 mL,反应完全后,过量的氢氧化钠用
0.100 0 mol/L盐酸滴定至终点,耗用盐酸20.16 mL,则0.100 0 g该试样中含CuSO4·5H2O_____________g。
(4)上述滴定中,滴定管在注入盐酸之前,先用蒸馏水洗净,再用_____________。

根据题意完成下列填空:
(1)向含铜粉的稀硫酸中滴加浓硝酸,在铜粉溶解时可以观察到的实验现象:_____________、_____________。
(2)如果铜粉、硫酸及硝酸都比较纯净,则制得的CuSO4·5H2O中可能存在的杂质是_____________,除去这种杂质的实验操作称为_____________。
(3)已知:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4。称取0.100 0 g提纯后的CuSO4·5H2O试样于锥形瓶中,加入0.100 0 mol/L氢氧化钠溶液28.00 mL,反应完全后,过量的氢氧化钠用
0.100 0 mol/L盐酸滴定至终点,耗用盐酸20.16 mL,则0.100 0 g该试样中含CuSO4·5H2O_____________g。
(4)上述滴定中,滴定管在注入盐酸之前,先用蒸馏水洗净,再用_____________。
(1)铜粉溶解,溶液呈蓝色 有红棕色气体产生
(2)Cu(NO3)2 重结晶 (3)0.098 0
(4)标准盐酸润洗2~3次
(2)Cu(NO3)2 重结晶 (3)0.098 0
(4)标准盐酸润洗2~3次
(1)铜和浓硝酸反应的化学方程式为:Cu+4HNO3(浓)=Cu(NO3)2+
2NO2↑+2H2O,其反应现象是铜逐渐溶解,溶液变蓝,产生红棕色气体。加入稀硫酸的目的是H+和Cu(NO3)2中的 结合成HNO3,继续和铜反应,尽可能地降低溶液中
结合成HNO3,继续和铜反应,尽可能地降低溶液中 的含量,得到纯净的CuSO4。(2)CuSO4·5H2O中可能存在少量的Cu(NO3)2杂质,它和CuSO4一样都易溶于水,可以利用它们的溶解度随温度的变化程度不同,采用重结晶的方法分离提纯。(3)跟CuSO4反应的n(NaOH)=0.100 0 mol/L×(0.028 00 L-0.020 16 L)=7.84×10-4 mol,n(CuSO4)=
的含量,得到纯净的CuSO4。(2)CuSO4·5H2O中可能存在少量的Cu(NO3)2杂质,它和CuSO4一样都易溶于水,可以利用它们的溶解度随温度的变化程度不同,采用重结晶的方法分离提纯。(3)跟CuSO4反应的n(NaOH)=0.100 0 mol/L×(0.028 00 L-0.020 16 L)=7.84×10-4 mol,n(CuSO4)= n(NaOH)=3.92×
n(NaOH)=3.92×
10-4 mol,m(CuSO4·5H2O)=3.92×10-4 mol×250 g/mol=0.098 0 g。(4)滴定管在注入盐酸之前,先用蒸馏水洗净,再用标准盐酸润洗2~3次
2NO2↑+2H2O,其反应现象是铜逐渐溶解,溶液变蓝,产生红棕色气体。加入稀硫酸的目的是H+和Cu(NO3)2中的
 结合成HNO3,继续和铜反应,尽可能地降低溶液中
结合成HNO3,继续和铜反应,尽可能地降低溶液中 的含量,得到纯净的CuSO4。(2)CuSO4·5H2O中可能存在少量的Cu(NO3)2杂质,它和CuSO4一样都易溶于水,可以利用它们的溶解度随温度的变化程度不同,采用重结晶的方法分离提纯。(3)跟CuSO4反应的n(NaOH)=0.100 0 mol/L×(0.028 00 L-0.020 16 L)=7.84×10-4 mol,n(CuSO4)=
的含量,得到纯净的CuSO4。(2)CuSO4·5H2O中可能存在少量的Cu(NO3)2杂质,它和CuSO4一样都易溶于水,可以利用它们的溶解度随温度的变化程度不同,采用重结晶的方法分离提纯。(3)跟CuSO4反应的n(NaOH)=0.100 0 mol/L×(0.028 00 L-0.020 16 L)=7.84×10-4 mol,n(CuSO4)= n(NaOH)=3.92×
n(NaOH)=3.92×10-4 mol,m(CuSO4·5H2O)=3.92×10-4 mol×250 g/mol=0.098 0 g。(4)滴定管在注入盐酸之前,先用蒸馏水洗净,再用标准盐酸润洗2~3次

练习册系列答案
相关题目

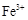 和
和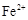 浓度相等。则已反应的
浓度相等。则已反应的