题目内容
【题目】物质的组成与结构决定了物质的性质与变化,回答下列问题:
(1)量子力学把电子在原子核外的一个空间运动状态称为一个____________,电子除空间运动状态外,还有一种运动状态叫做____________。
(2)硒常用作光敏材料,基态硒原子的价电子排布式为_______________;与硒同周期的p区元素中第一电离能大于硒的元素有_________种。
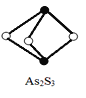
(3)成语“信口雌黄”中的雌黄分子式为As2S3,分子结构如下图,As原子的杂化方式为___________,雌黄和SnCl2在盐酸中反应转化为雄黄(As4S4)和SnCl4并放出H2S气体,写出该反应方程式________________。SnCl4分子的空间构型为_______。
(4)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如图。

①储氢原理为:镧镍合金吸附H2,H2解离为原子,H储存在其中形成化合物。若储氢后,氢原子占据晶胞中上下底面的棱和面心则形成的储氢化合物的化学式为_________。
②测知镧镍合金晶胞体积为9.0×10-23cm3,则镧镍合金的晶体密度为_______。(不必计算出结果,用NA表示阿伏伽德罗常数。)
【答案】 原子轨道 自旋 4s24p4 3 sp3杂化 2As2S3+2 SnCl2+4HCl = As4S4 + 2 SnCl4+2H2S↑ 正四面体形 LaNi5H3 ![]()
【解析】(1)量子力学把电子在原子核外的一个空间运动状态称为一个原子轨道,电子除空间运动状态外,还有一种运动状态叫做自旋。
(2)Se原子序数为34,电子排布式:1s22s22p63s23p63d104s24p4,基态硒原子的价电子排布式:4s24p4 。第四周期元素中第一电离能大于硒的元素有溴、砷
和氪,共3 种。
(3)雌黄分子式为As2S3,根据分子结构图可分析,As原子的杂化方式为:sp3杂化;根据反应物和生成物:As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体,可以得出化学方程式为:2As2S3+2SnCl2+4HCl=As4S4+2SnCl4+2H2S↑;
SnCl4分子sp3杂化 ,空间构型为正四面体。
(4)①镧镍合金吸附H2,H2解离为原子,H储存在其中形成化合物,La的原子个数= 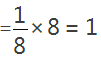 ,Ni的原子个数
,Ni的原子个数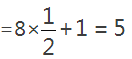 ,所以该合金的化学式为LaNi5,储氢后,氢原子占据晶胞中上下底面的棱和面心,则H的原子个数=(8╳1/4)+1=3,故答案为:LaNi5H3。②测知镧镍合金晶胞体积为9.0×10-23cm3,则镧镍合金的晶体密度为
,所以该合金的化学式为LaNi5,储氢后,氢原子占据晶胞中上下底面的棱和面心,则H的原子个数=(8╳1/4)+1=3,故答案为:LaNi5H3。②测知镧镍合金晶胞体积为9.0×10-23cm3,则镧镍合金的晶体密度为![]()

 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案