题目内容
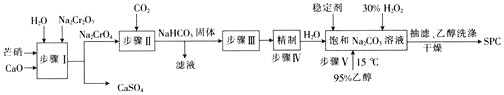
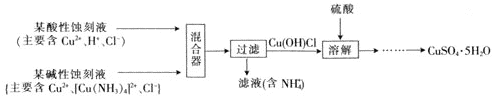
【题目】利用水钴矿(主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、MgO、CaO、SiO2等)可以制取多种化工试剂,以下为草酸钴晶体和氯化钴晶体的制备流程,回答下列问题:
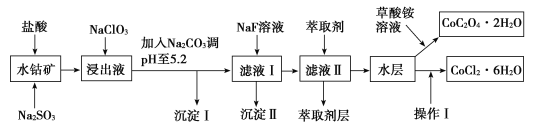
已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+、Mg2+、Ca2+等。
②沉淀Ⅰ中只含有两种沉淀。
③流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
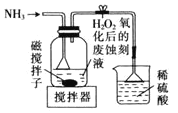
(1)浸出过程中加入Na2SO3目的是___。
(2)NaClO3在浸出液中发生反应的离子方程式为___。
(3)加入Na2CO3调pH至5.2,目的是___;萃取剂层含锰元素,则沉淀Ⅱ的主要成分为__。
(4)操作Ⅰ包括:将水层加入浓盐酸调整pH为2~3,___、__、过滤、洗涤、减压烘干等过程。
(5)为测定粗产品中CoCl2·6H2O的含量,称取一定质量的粗产品溶于水,加入足量硝酸酸化的硝酸银溶液,过滤、洗涤、干燥,测沉淀质量。通过计算发现粗产品中CoCl2·6H2O质量分数大于100%,其原因可能是___(回答一条原因即可)。
(6)将5.49g草酸钴晶体(CoC2O4·2H2O)置于空气中加热,受热过程中不同温度范围内分别得到一种固体物质,其质量如下表。
温度范围/℃ | 固体质量/g |
150~210 | 4.41 |
290~320 | 2.41 |
经测定,整个受热过程,只产生水蒸气和CO2气体,则290~320℃温度范围,剩余的固体物质化学式为____。[已知:CoC2O4·2H2O的摩尔质量为183g·mol1]
【答案】将Fe3+、Co3+还原 ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O 使Fe3+和Al3+沉淀完全 CaF2和MgF2 蒸发浓缩 冷却结晶 粗产品中结晶水含量低(或粗产品中混有氯化钠杂质) Co3O4(或CoO·Co2O3)
【解析】
(1)、浸出过程中,Co2O3、Fe2O3与盐酸、Na2SO3发生反应,Co2O3转化为Co2+,Fe2O3转化为Fe2+,Co、Fe元素化合价降低,则S元素化合价升高,SO32-转化为SO42-,故答案为:将Fe3+、Co3+还原;
(2)、NaClO3加入浸出液中,将Fe2+氧化为Fe3+,ClO-被还原为Cl-,反应的离子方程式为:ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O-;
(3)根据工艺流程图结合表格中提供的数据可知,加Na2CO3调pH至5.2,目的是使Fe3+和Al3+沉淀完全。滤液l中含有的金属阳离子为Co2+、Mn2+、Mg2+、Ca2+等,萃取剂层含锰元素,结合流程图中向滤液1中加入了NaF溶液,知沉淀Ⅱ为MgF2、CaF2;
(4)、经过操作I由溶液得到结晶水合物,故除题中已知过程外,操作I还包括蒸发浓缩、冷却结晶;
(5)、根据CoCl2·6H2O的组成及测定过程分析,造成粗产品中CoCl2·6H2O的质量分数大于100%的原因可能是:含有氯化钠杂质,使氯离子含量增大或结晶水合物失去部分结晶水,导致相同质量的固体中氯离子含量变大;
(6)、整个受热过程中只产生水蒸气和CO2气体,5.49 g CoC2O4·2H2O为0.03mol,固体质量变为4.41 g时,质量减少1.08g,恰好为0.06 mol H2O的质量,因此4.41 g固体为0.03 mol CoC2O4。依据元素守恒知,生成n(CO2)=0.06 mol,m(CO2)=0.06mol×44 g/mol=2.64 g。而固体质量由4.41 g变为2.41 g时,质量减少2 g,说明290~320℃内发生的不是分解反应,参加反应的物质还有氧气。则参加反应的m(O2)=2.64 g-2 g=0.64 g,n(O2)=0.02mol,n(CoC2O4) : n(O2) : n(CO2)=0.03 : 0.02 : 0.06=3 : 2 : 6,依据原子守恒,配平化学方程式![]() ,故290~320℃温度范围,剩余固体物质的化学式为Co3O4或CoO·Co2O3。
,故290~320℃温度范围,剩余固体物质的化学式为Co3O4或CoO·Co2O3。

【题目】铈(Ce)是![]() 种重要的稀土元素。以富含CeO2的废玻璃粉末(含SiO2、Fe2O3以及其他少量可溶于稀酸的杂质)为原料,采用多种方法回收铈。请回答下列问题:
种重要的稀土元素。以富含CeO2的废玻璃粉末(含SiO2、Fe2O3以及其他少量可溶于稀酸的杂质)为原料,采用多种方法回收铈。请回答下列问题:

已知:CeO2不溶于稀盐酸,也不溶于NaOH溶液。
⑴滤渣的成分是________,反应②的离子方程式是________。
⑵干法空气氧化法回收铈是把Ce(OH)3被空气氧化成Ce(OH)4,氧化过程中发生的化学反应方程式为________。两种制备Ce(OH)4的数据如下表:
干法空气氧化法 | 氧化温度 | 氧化率 | 氧化时间 |
暴露空气中 | 110~120 | 90 | 18 |
在对流空气氧化炉中 | 110~120 | 99 | 8 |
在对流空气氧化炉中大大缩短氧化时间的原因是________。
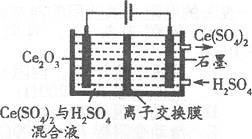
⑶利用电解方法也可以实现铈的回收。
①在酸性条件下电解Ce2O3(如图):阳极电极反应式为________,离子交换膜为________(填“阴”或“阳”)离子交换膜。
②电解产物Ce(SO4)2是重要的氧化剂,将其配成标准溶液,在酸性条件下能测定工业盐中NaNO2的含量,写出发生反应的离子方程式________。