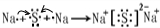题目内容
A、B、C、D是四种短周期元素,它们的原子序数依次增大,其中A与C,B与D分别是同主族元素;已知B、D二元素原子核中质子数之和是A、C二元素原子核中质子数之和的2倍;四种元素形成的单质中有两种是气体,两种是固体.请回答以下问题:(1)写出由A、B两元素形成的原子个数比为1:1的化合物的化学式______,此化合物能使酸性KMnO4溶液退色,体现该化合物具有______性.
(2)D元素在元素周期表中的位置______,B和C两元素形成的原子个数比为1:1的化合物中含有的化学键的类型为______.
(3)A、B、C、D四种原子半径由大到小为______(填元素符号);四种离子半径由大到小为______(填离子符号).
(4)写出由A、B两元素形成的原子个数比为2:1的化合物与B、C两元素形成的原子个数比为1:1的化合物反应的离子方程式______.
(5)两种物质均由A、B、C、D四种元素组成,写出它们在水溶液中反应的离子方程式______.
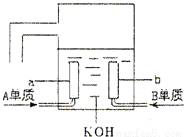
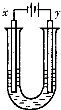
(6)用A元素的单质与B元素的单质可制成新型的化学电源,已在宇宙飞船中使用.其构造如图所示.两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电.则a是______极,电极反应式为______,b是______极,电极反应式为______.
【答案】分析:A、B、C、D原子序数依次增大短周期元素,A、C及B、D分别是同一主族元素,确定B、D分别位于二、三周期;由于B、D两元素的原子核中质子数之和是A、C两元素原子核中质子数之和的两倍,确定A、C分别位于一、三周期,所以A为氢、C为钠、B为氧、D为硫.
解答:解:A、B、C、D原子序数依次增大短周期元素,A、C及B、D分别是同一主族元素,确定B、D分别位于二、三周期;由于B、D两元素的原子核中质子数之和是A、C两元素原子核中质子数之和的两倍,确定A、C分别位于一、三周期,所以A为氢、C为钠、B为氧、D为硫.
(1)由A、B两元素形成的原子个数比为1:1的化合物为H2O2,H2O2能使酸性KMnO4溶液退色,H2O2被酸性KMnO4溶液氧化,体现酸性H2O2的还原性.
故答案为:H2O2;还原性.
(2)D为硫,处于周期表中第三周期第ⅥA族;B和C两元素形成的原子个数比为1:1的化合物为Na2O2,由钠离子与过氧根离子构成,钠离子与过氧根离子之间形成离子键,过氧根离子中氧原子之间形成共价键.
故答案为:第三周期第ⅥA族;离子键、共价键.
(3)同周期自左而右原子半径减小,电子层越大原子半径越大,所以原子半径Na>S>O>H;最外层电子数相同,电子层越多离子半径越大,电子层结构相同,核电荷数越大离子半径越小,H+半径最小,所以S2->O2->Na+>H+.
故答案为:Na>S>O>H;S2->O2->Na+>H+.
(4)由A、B两元素形成的原子个数比为2:1的化合物为H2O,由B、C两元素形成的原子个数比为1:1的化合物为Na2O2,过氧化钠与水反应生成氢氧化钠与氧气,反应的离子方程式为2Na2O2+2H2O=4Na++4OH-+O2↑.
故答案为:2Na2O2+2H2O=4Na++4OH-+O2↑.
(5)两种均含A,B,C,D四种元素的化合物相互间发生反应,且生成气体,为亚硫酸氢钠与硫酸氢钠反应,生成二氧化硫与水,反应离子方程式为HSO3-+H+=SO2↑+H2O.
故答案为:HSO3-+H+=SO2↑+H2O.
(6)氢氧碱性燃料电池,负极发生氧化反应,氢气在负极放电,a为负极,电极反应式为4H2-4e-=4H+,正极发生还原反应,氧气在正极放电,b为正极,电极反应式O2+2H2O+4e-=4OH-.
故答案为:负,4H2-4e-=4H+;正,O2+2H2O+4e-=4OH-.
点评:考查学生利用原子的结构来推断元素、常用化学用语、原电池等,难度较大,注意本题中利用A、C与B、D可能存在情况来分析是推断难点.
解答:解:A、B、C、D原子序数依次增大短周期元素,A、C及B、D分别是同一主族元素,确定B、D分别位于二、三周期;由于B、D两元素的原子核中质子数之和是A、C两元素原子核中质子数之和的两倍,确定A、C分别位于一、三周期,所以A为氢、C为钠、B为氧、D为硫.
(1)由A、B两元素形成的原子个数比为1:1的化合物为H2O2,H2O2能使酸性KMnO4溶液退色,H2O2被酸性KMnO4溶液氧化,体现酸性H2O2的还原性.
故答案为:H2O2;还原性.
(2)D为硫,处于周期表中第三周期第ⅥA族;B和C两元素形成的原子个数比为1:1的化合物为Na2O2,由钠离子与过氧根离子构成,钠离子与过氧根离子之间形成离子键,过氧根离子中氧原子之间形成共价键.
故答案为:第三周期第ⅥA族;离子键、共价键.
(3)同周期自左而右原子半径减小,电子层越大原子半径越大,所以原子半径Na>S>O>H;最外层电子数相同,电子层越多离子半径越大,电子层结构相同,核电荷数越大离子半径越小,H+半径最小,所以S2->O2->Na+>H+.
故答案为:Na>S>O>H;S2->O2->Na+>H+.
(4)由A、B两元素形成的原子个数比为2:1的化合物为H2O,由B、C两元素形成的原子个数比为1:1的化合物为Na2O2,过氧化钠与水反应生成氢氧化钠与氧气,反应的离子方程式为2Na2O2+2H2O=4Na++4OH-+O2↑.
故答案为:2Na2O2+2H2O=4Na++4OH-+O2↑.
(5)两种均含A,B,C,D四种元素的化合物相互间发生反应,且生成气体,为亚硫酸氢钠与硫酸氢钠反应,生成二氧化硫与水,反应离子方程式为HSO3-+H+=SO2↑+H2O.
故答案为:HSO3-+H+=SO2↑+H2O.
(6)氢氧碱性燃料电池,负极发生氧化反应,氢气在负极放电,a为负极,电极反应式为4H2-4e-=4H+,正极发生还原反应,氧气在正极放电,b为正极,电极反应式O2+2H2O+4e-=4OH-.
故答案为:负,4H2-4e-=4H+;正,O2+2H2O+4e-=4OH-.
点评:考查学生利用原子的结构来推断元素、常用化学用语、原电池等,难度较大,注意本题中利用A、C与B、D可能存在情况来分析是推断难点.

练习册系列答案
相关题目
a、b、c、d是四种短周期元素.a、b、d同周期,c、d同主族.a的原子结构示意图为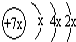 ,b与c形成化合物的电子式为
,b与c形成化合物的电子式为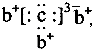 下列比较中正确的是( )
下列比较中正确的是( )
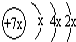 ,b与c形成化合物的电子式为
,b与c形成化合物的电子式为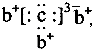 下列比较中正确的是( )
下列比较中正确的是( )| A、原子半径:a>c>d>b | B、最高价含氧酸的酸性c>d>a | C、原子序数:a>d>b>c | D、单质的氧化性a>b>d>c |
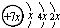 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题: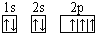

 Al(OH)3+OH-
Al(OH)3+OH-