��Ŀ����
��ȸʯ��Ҫ��Cu2 (OH)2CO3����������Fe��Si�Ļ����ij�����Կ�ȸʯΪ��Ҫԭ���Ʊ�CuSO4��5 H2O�����ײ���G����Ҫ�������£�
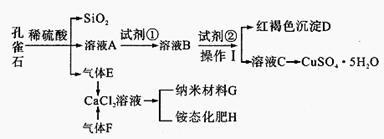
��֪�������£�ͨ��������Һ������Զ�ʹFe3+��Fe2+��Cu2+���ɳ�����pH�ֱ����£�
��ش��������⣺
��1��д����ȸʯ��Ҫ�ɷ�Cu2(OH)2CO3��ϡ���ᷴӦ�Ļ�ѧ����ʽ���������� ����������������
��2����ҺA�Ľ���������Cu2+��Fe2+��Fe3+��Ҫ�������е�Fe2+Ӧѡ�������Լ��е� ��
a��KMnO4 b��NaOH c��H2O2 d��KSCN
��3����ҺA�еĽ���������Cu2+��Fe2+��Fe3+���Լ�����һ������������Fe2+������Fe3+��Ŀ���� ���ù���ѡ���Լ������Ϊ�����е� ������ţ���
a��H2O2 b������ c��Cl2 d��KSCN
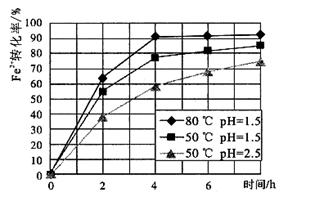
��4��������ͼ�й����ݣ�����Ϊ��ҵ����������ʱӦ��ȡ�Ĵ�ʩ�� ��
��5������ҺB�м����Լ��ڵĻ�ѧʽΪ ������I�������� ��
��6������E������FӦ����ͨ��CaCl2��Һ�е��� ���ѧʽ����д���Ʊ�G��H�Ļ�ѧ��Ӧ����ʽ ��
��7�����ⶨ��ҺA��Fe2+��Ũ�ȣ�����KMnO4����Һ�ζ�����Ӧ��MnO4����ԭΪMn2+����÷�Ӧ�����ӷ���ʽΪ �������������������������������� ��ȡA��Һ20.00 mL����ȥ0.0240mol��LKMnO4��Һ16.00 mLʱ��ǡ�ôﵽ�ζ��յ㣬��A��Һ��Fe2+Ũ��Ϊ ��

��֪�������£�ͨ��������Һ������Զ�ʹFe3+��Fe2+��Cu2+���ɳ�����pH�ֱ����£�
| ���� | ��ʼ����ʱ��pH | ��ȫ����ʱ��pH |
| Fe(OH)3 | 2.2 | 3.2 |
| Fe(OH)2 | 7.6 | 9.6 |
| Cu(OH)2 | 4.7 | 6.4 |
��1��д����ȸʯ��Ҫ�ɷ�Cu2(OH)2CO3��ϡ���ᷴӦ�Ļ�ѧ����ʽ���������� ����������������
��2����ҺA�Ľ���������Cu2+��Fe2+��Fe3+��Ҫ�������е�Fe2+Ӧѡ�������Լ��е� ��
a��KMnO4 b��NaOH c��H2O2 d��KSCN
��3����ҺA�еĽ���������Cu2+��Fe2+��Fe3+���Լ�����һ������������Fe2+������Fe3+��Ŀ���� ���ù���ѡ���Լ������Ϊ�����е� ������ţ���
a��H2O2 b������ c��Cl2 d��KSCN
��4��������ͼ�й����ݣ�����Ϊ��ҵ����������ʱӦ��ȡ�Ĵ�ʩ�� ��

��5������ҺB�м����Լ��ڵĻ�ѧʽΪ ������I�������� ��
��6������E������FӦ����ͨ��CaCl2��Һ�е��� ���ѧʽ����д���Ʊ�G��H�Ļ�ѧ��Ӧ����ʽ ��
��7�����ⶨ��ҺA��Fe2+��Ũ�ȣ�����KMnO4����Һ�ζ�����Ӧ��MnO4����ԭΪMn2+����÷�Ӧ�����ӷ���ʽΪ �������������������������������� ��ȡA��Һ20.00 mL����ȥ0.0240mol��LKMnO4��Һ16.00 mLʱ��ǡ�ôﵽ�ζ��յ㣬��A��Һ��Fe2+Ũ��Ϊ ��
��1��Cu2(OH)2CO3+2H2SO4��2CuSO4+3H2O+CO2����2�֣�
��2��a��1�֣�
��3��������Һ��PHʱ��Fe3+��Cu2+��ʼ����֮ǰ���ܳ�����ȫ���Ӷ��������ʳ�ȥ��1�֣�
a��1�֣�
��4����Һ�¶ȿ�����80�棬PH������1.5������ʱ��Ϊ4Сʱ���ң�1�֣�
��5��CuO��1�֣� ���ˣ�1�֣�
��6��NH3��1�֣� 2NH3+CO2+CaCl2+H2O==CaCO3��+2NH4Cl��2�֣�
��7��MnO4��+ 5Fe2+ + 8H+="==" Mn2+ + 5Fe3+ + 4H2O��2�֣� 0.0960mol/L��2�֣�
��2��a��1�֣�
��3��������Һ��PHʱ��Fe3+��Cu2+��ʼ����֮ǰ���ܳ�����ȫ���Ӷ��������ʳ�ȥ��1�֣�
a��1�֣�
��4����Һ�¶ȿ�����80�棬PH������1.5������ʱ��Ϊ4Сʱ���ң�1�֣�
��5��CuO��1�֣� ���ˣ�1�֣�
��6��NH3��1�֣� 2NH3+CO2+CaCl2+H2O==CaCO3��+2NH4Cl��2�֣�
��7��MnO4��+ 5Fe2+ + 8H+="==" Mn2+ + 5Fe3+ + 4H2O��2�֣� 0.0960mol/L��2�֣�
��1��Cu2(OH)2CO3���ڼ�ʽ�Σ���ϡ���ᷴӦ��������ͭ��CO2��ˮ����ӦʽΪCu2(OH)2CO3+2H2SO4��2CuSO4+3H2O+CO2����
��2���������Ӿ��л�ԭ�ԣ���ʹ���Ը��������Һ��ɫ�����Կ�ѡ��a��
��3��Ҫ�Ʊ�����ͭ��������ȥ�����Ӻ��������ӡ����ݱ������ݿ�֪Ҫͨ��������ֱ�ӳ�ȥ�������ӣ���ͭ����Ҳ����ͬʱ��ȥ������Ӧ�ð����������������������ӣ�Ȼ����ͨ���������������ӡ���Ϊ������������ȫ������ͭ���ӻ�������Һ�С���ѡ��������������������µ����ʣ�����Ӧ��ѡ����ɫ������˫��ˮ��
��4������ͼ���֪����80��pH����1.5ʱת������ߣ�����Ӧ�ÿ��Ƶ�����������Һ�¶ȿ�����80�棬PH������1.5������ʱ��Ϊ4Сʱ���ҡ�
��5��Ҫ�õ�������������������������Һ��pH��ͬʱ�������������ʣ����Կ�ѡ������ͭ��Ҫ�����Һ������Ҫ���ˡ�
��6��E��CO2��CO2���Ȼ����Dz���Ӧ�ģ�Ҫ�õ�̼��Ƴ������ͽ�����Һ�����ԣ��������ͨ�백����ʹ��Һ�Լ��ԣ�Ȼ����ͨ��CO2��������̼��ƺ��Ȼ�李���ӦʽΪ2NH3+CO2+CaCl2+H2O==CaCO3��+2NH4Cl��
��7���μӷ�Ӧ�ĸ��������0.0240mol��L��0.016L��0.000384mol��������������������ӵķ���ʽΪMnO4��+ 5Fe2+ + 8H+="==" Mn2+ + 5Fe3+ + 4H2O���������ĵ���������Ϊ0.000384mol��5��0.00192mol������Ũ��Ϊ ��
��
��2���������Ӿ��л�ԭ�ԣ���ʹ���Ը��������Һ��ɫ�����Կ�ѡ��a��
��3��Ҫ�Ʊ�����ͭ��������ȥ�����Ӻ��������ӡ����ݱ������ݿ�֪Ҫͨ��������ֱ�ӳ�ȥ�������ӣ���ͭ����Ҳ����ͬʱ��ȥ������Ӧ�ð����������������������ӣ�Ȼ����ͨ���������������ӡ���Ϊ������������ȫ������ͭ���ӻ�������Һ�С���ѡ��������������������µ����ʣ�����Ӧ��ѡ����ɫ������˫��ˮ��
��4������ͼ���֪����80��pH����1.5ʱת������ߣ�����Ӧ�ÿ��Ƶ�����������Һ�¶ȿ�����80�棬PH������1.5������ʱ��Ϊ4Сʱ���ҡ�
��5��Ҫ�õ�������������������������Һ��pH��ͬʱ�������������ʣ����Կ�ѡ������ͭ��Ҫ�����Һ������Ҫ���ˡ�
��6��E��CO2��CO2���Ȼ����Dz���Ӧ�ģ�Ҫ�õ�̼��Ƴ������ͽ�����Һ�����ԣ��������ͨ�백����ʹ��Һ�Լ��ԣ�Ȼ����ͨ��CO2��������̼��ƺ��Ȼ�李���ӦʽΪ2NH3+CO2+CaCl2+H2O==CaCO3��+2NH4Cl��
��7���μӷ�Ӧ�ĸ��������0.0240mol��L��0.016L��0.000384mol��������������������ӵķ���ʽΪMnO4��+ 5Fe2+ + 8H+="==" Mn2+ + 5Fe3+ + 4H2O���������ĵ���������Ϊ0.000384mol��5��0.00192mol������Ũ��Ϊ
 ��
��
��ϰ��ϵ�д�
 ���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д�
���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д� ����ѵ��ϵ�д�
����ѵ��ϵ�д�
�����Ŀ
 ________________
________________